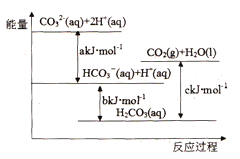
��Ŀ����
����Ŀ��ʵ�����Ա�����ȩΪԭ�ϣ����Ȼ���Ϊ�������Ʊ�1��1���������飬�䷴Ӧԭ��Ϊ��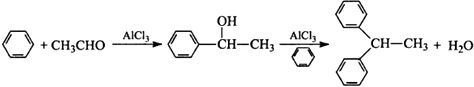
�Ʊ������������������AlCl3��������Ӧ����Ҫʵ��װ�úͲ������£�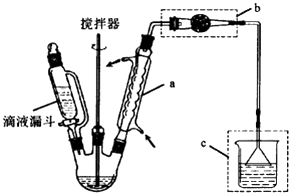
I���ϳɣ�
��250mL������ƿ�м���140mL�����ܶ�0.88g/mL����19gA1C13��5.5g��ȩ����20��ʱ��ַ�Ӧ��
�������ᴿ��
����Ӧ����ﵹ��װ��150mL����ˮ������������ձ��У���ֽ��裬�÷�Һ©��������л��㣬������ˮ��2%̼������Һ��ˮϴ�ӣ��ڷ�����Ĵֲ�Ʒ�м���������ˮ����þ���壬���˺��ȳ�ѹ�����ȥ�������ٸ��ü�ѹ�����ռ�170��172��/6.67kPa����֣���12.5g 1��l���������飮
��1������a�����ƣ�������������A1C13��������Ӧ�Ļ�ѧ����ʽΪ����װ��C�����ã� ��
��2������װ��b�������� ��
��3����ϴ�Ӳ����У��ڶ���ˮϴ����ҪĿ���� �� ʵ���м���������ˮ����þ��Ŀ���� ��
��4���ֲ�Ʒ��ѹ�����ᴿʱ������װ�����¶ȼ�λ����ȷ���� �� ���ܻᵼ���ռ����IJ�Ʒ�л��еͷе����ʵ�װ���� �� 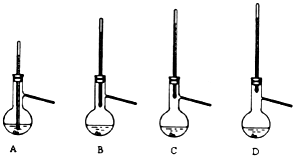
��5����ʵ�����õ���1��1�������������ԼΪ������ȷ�𰸵���ţ���
A.41%
B.48%
C.55%
D.65%
���𰸡�
��1�����������ܣ�AlCl3+3H2O?Al��OH��3+3HCl������HCl����
��2����ֹ�ձ��е�ˮ�������뷴Ӧ���������Ȼ�����Ӧ
��3��ϴ���Ȼ����������̼���Ƶȿ������������
��4��C��AB
��5��C
���������⣺��1���������ṹ��������֪����aΪ���������ܣ���Ӧ������ AlCl3�ᷢ��ˮ�⣬�ʻ����ɸ�����������������Ӧ����ʽΪ��AlCl3+3H2OAl��OH��3+3HCl��cװ������HCl���ĵ��õ�©���������ٽ�HCl��������գ���ֹ���������Դ��ǣ����������ܣ�AlCl3+3H2OAl��OH��3+3HCl������HCl���壻��2������ AlCl3�ᷢ��ˮ�⣬��ʵ������Ҫ��ֹˮ�� AlCl3��ˮ�Ӵ���װ��b������Ϊ����ֹ�ձ��е�ˮ�������뷴Ӧ���������Ȼ�����Ӧ�����Դ��ǣ���ֹ�ձ��е�ˮ�������뷴Ӧ���������Ȼ�����Ӧ����3���ڶ�����ˮϴ����Ϊ��ϴ���Ȼ����������̼���Ƶȿ����������ˮ����þ��Ϊ����������ˮ�����������ã����Դ��ǣ�ϴ���Ȼ����������̼���Ƶȿ�������������4������������¶ȼ�ˮ����λ��������ƿ��֧�ܿڴ�����ѡC�������¶ȼ�ˮ����ֱ�ӻ���֧�ܿ��·���ǰ�Ӵ����������ܻᵼ���ռ����IJ�Ʒ�л��еͷе����ʣ���AB�����Դ��ǣ�C��AB����5�������ʵ���Ϊ ![]() =1.58mol����ȩ���ʵ���Ϊ
=1.58mol����ȩ���ʵ���Ϊ ![]() =0.125mol���ɷ���ʽ��֪��n����ȩ��=n������������ȩ���㣬��n����ȩ��=n��1��l���������飩=0.125mol����������1��l���������������Ϊ��0.125mol��178g/mol=22.25g����ʵ������1��l����������Ϊ12.5g����1��l����������IJ���Ϊ��
=0.125mol���ɷ���ʽ��֪��n����ȩ��=n������������ȩ���㣬��n����ȩ��=n��1��l���������飩=0.125mol����������1��l���������������Ϊ��0.125mol��178g/mol=22.25g����ʵ������1��l����������Ϊ12.5g����1��l����������IJ���Ϊ�� ![]() ��100%=55%����ѡ��C��
��100%=55%����ѡ��C��