题目内容
【题目】实验室里需要纯净的NaCl溶液,但现在只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。
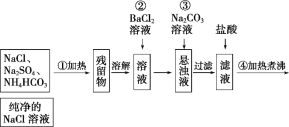
(已知:NH4HCO3![]() NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
如果此方案正确,回答下列问题:
(1)操作①可选择的主要仪器是____________、____________。
(2)操作②不用硝酸钡溶液,其理由是__________________________________________。
(3)进行操作②后,如何判断SO42 已除尽,方法是_________________________。
(4)操作③的目的是________________。
(5)操作④的目的是__________________________________________________。
【答案】坩埚(或蒸发皿或试管) 酒精灯 溶液中引入新的杂质离子NO3- 取少量上层清液加入BaCl2溶液,若无白色沉淀说明SO42-已除尽 除去过量的Ba2+ 除去溶解在溶液中的CO2和HCl
【解析】
混有硫酸钠、碳酸氢铵的氯化钠固体,由流程可知,①中加热条件下分解,分解后的固体溶于水后,与氯化钡反应除去硫酸根离子,再利用碳酸钠除去过量的钡离子,过滤后滤液中含NaCl、碳酸钠,加盐酸除去碳酸钠后溶质为NaCl,蒸发得到纯净的NaCl。
(1)用酒精灯加热固体,应在坩埚中进行。
(2)加入硝酸钡溶液和硫酸钠反应生成硫酸钡和硝酸钠,除去了硫酸根离子,但引入了硝酸根新的杂质离子;
(3)加入过量氯化钡溶液,如果硫酸根离子没有完全除去,能够与钡离子反应生成沉淀,所以检验硫酸根离子已除尽,可静置片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽;故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有;
(4)加入碳酸钠,可用于除去过量的Ba2+,反应的化学方程式为Na2CO3+BaCl2=BaCO3↓+2 NaCl;
(5)操作④加热煮沸溶液的目的是除去滤液中溶解的二氧化碳和多余的氯化氢。

 名校课堂系列答案
名校课堂系列答案