题目内容
【题目】(1)有pH均为2的a盐酸、b醋酸两瓶溶液,与足量锌反应放出等体积H2所需时间的长短顺序是a____b(用“>”、“<”、“=”表示,下同);完全中和等物质的量的NaOH溶液需两种酸的体积大小顺序是a____b。
(2)已知水在25℃和95℃时,其电离平衡曲线如下图所示:
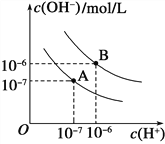
①则25℃时水的电离平衡曲线应为________(填“A”或“B”)。
②95℃时水的离子积KW=___________________。
③25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为____________。
④95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_____________。
【答案】>>A1×10-1210:1pH1+pH2=14或a+b=14
【解析】(1)醋酸为弱酸,等pH时醋酸的浓度较大,与锌反应时醋酸的速率大,则生成等体积的氢气,盐酸反应的时间较长,完全中和等物质的量的NaOH溶液,需要醋酸的体积较小;
(2)①曲线A条件下Kw=c(H+)×c(OH-)=10-7×10-7=10-14,曲线B条件下c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+)c(OH-)=10-12 ;水的电离时吸热过程,加热促进电离,所以A曲线代表25℃时水的电离平衡曲线;
②B为95℃水的电离平衡曲线,纯水中c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+)c(OH-)=10-12 ;
③25℃时所得混合溶液的pH=7,溶液呈中性即酸碱恰好中和,即n(OH-)=n(H+),则V(NaOH)10-5 molL-1=V(H2SO4)10-4 molL-1,得V(NaOH):V(H2SO4)=10:1;
④强酸的pH=a,强碱的pH=b,由95℃时,若100体积的某强酸溶液与1体积的某强碱溶液混和后溶液呈中性,即n(H+)=n(OH-),则100×10-a=1×10b-12,102-a=10b-12,即2-a=b-12,则a+b=14。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案