题目内容
【题目】我国的矿产资源丰富。利用某冶炼废渣(主要成分为二氧化硅和锡、铜、铅、铁的氧化物)回收锡、铜、铅的工艺流程如下图所示:

回答下列问题:
(1)电炉冶炼时,焦炭的作用是________(填“氧化剂”或“还原剂”),将焦炭粉碎的目的是__________。熔剂的主要成分是氟石(CaF2),高温下能与SiO2反应生成两种钙盐,其中之一为 CaSiF6,该反应的化学方程式为____________________________。![]()
(2)脱铁后的溶液中含有少量的Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为____________________________。
(3)已知SnO2不溶于稀硫酸。脱铁后氧化焙烧的目的是__________________。
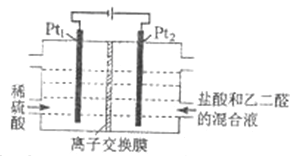
(4)电解CuSO4溶液时,阳极的电极反应式为___________________________。
(5)已知H2CO3的一、二级电离常数分别为K1、K2,PbSO4、PbCO3的溶度积常数分别为Ksp(PbSO4)、Ksp(PbCO3)。锡、铅渣中的铅主要以PbSO4存在,脱硫时发生的反应为:
PbSO4(s)+HCO3ˉ(aq) ![]() PbCO3(s)+H+(aq)+SO42-(aq),该反应的平衡常数K=___________(用上述已知常数表示)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是_____________________________。
PbCO3(s)+H+(aq)+SO42-(aq),该反应的平衡常数K=___________(用上述已知常数表示)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是_____________________________。
(6)若该冶炼废渣中锡的质量分数为5%,30t废渣制得精锡lt,则锡的回收率为_____________________。
【答案】 还原剂 加快反应速率使反应更充分 3CaF2+3SiO2 ![]() CaSiF6+2CaSiO3 Sn2++Fe=Sn+Fe2+ 将Sn、Cu分别氧化为SnO2、CuO,利于浸铜时分离 2H2O-4e-=O2↑+4H+
CaSiF6+2CaSiO3 Sn2++Fe=Sn+Fe2+ 将Sn、Cu分别氧化为SnO2、CuO,利于浸铜时分离 2H2O-4e-=O2↑+4H+ ![]() 取少量末次洗涤液于试管中,滴加氯化钡溶液,若不出现浑浊,说明滤渣已洗净(合理答案均可) 66.7%
取少量末次洗涤液于试管中,滴加氯化钡溶液,若不出现浑浊,说明滤渣已洗净(合理答案均可) 66.7%
【解析】(1)电炉冶炼时,焦炭将金属氧化物还原产生合金,焦炭的作用是还原剂,将焦炭粉碎的目的是加快反应速率使反应更充分。熔剂的主要成分是氟石(CaF2),高温下能与SiO2反应生成两种钙盐,其中之一为 CaSiF6,该反应的化学方程式为3CaF2+3SiO2![]() CaSiF6+2CaSiO3;(2)脱铁后的溶液中含有少量的Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,利用铁金属性强于锡置换出锡,反应的离子方程式为Sn2++Fe=Sn+Fe2+;(3)已知SnO2不溶于稀硫酸。脱铁后氧化焙烧的目的是将Sn、Cu分别氧化为SnO2、CuO,利于浸铜时分离;(4)电解CuSO4溶液时,阳极水电离出的氢氧根离子失电子产生氧气,反应的电极反应式为2H2O-4e-=O2↑+4H+;(5)已知H2CO3的一、二级电离常数分别为K1、K2,PbSO4、PbCO3的溶度积常数分别为Ksp(PbSO4)、Ksp(PbCO3)。锡、铅渣中的铅主要以PbSO4存在,脱硫时发生的反应为PbSO4(s)+HCO3ˉ(aq)
CaSiF6+2CaSiO3;(2)脱铁后的溶液中含有少量的Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,利用铁金属性强于锡置换出锡,反应的离子方程式为Sn2++Fe=Sn+Fe2+;(3)已知SnO2不溶于稀硫酸。脱铁后氧化焙烧的目的是将Sn、Cu分别氧化为SnO2、CuO,利于浸铜时分离;(4)电解CuSO4溶液时,阳极水电离出的氢氧根离子失电子产生氧气,反应的电极反应式为2H2O-4e-=O2↑+4H+;(5)已知H2CO3的一、二级电离常数分别为K1、K2,PbSO4、PbCO3的溶度积常数分别为Ksp(PbSO4)、Ksp(PbCO3)。锡、铅渣中的铅主要以PbSO4存在,脱硫时发生的反应为PbSO4(s)+HCO3ˉ(aq) ![]() PbCO3(s)+H+(aq)+SO42+(aq),该反应的平衡常数K=
PbCO3(s)+H+(aq)+SO42+(aq),该反应的平衡常数K=![]() ;检验滤渣是否洗涤干净是检验洗涤液中是否含有硫酸根离子,检验的方法是取少量末次洗涤液于试管中,滴加氯化钡溶液,若不出现浑浊,说明滤渣已洗净;(6)若该冶炼废渣中锡的质量分数为5%,30t废渣制得精锡lt,则锡的回收率为
;检验滤渣是否洗涤干净是检验洗涤液中是否含有硫酸根离子,检验的方法是取少量末次洗涤液于试管中,滴加氯化钡溶液,若不出现浑浊,说明滤渣已洗净;(6)若该冶炼废渣中锡的质量分数为5%,30t废渣制得精锡lt,则锡的回收率为![]() 。
。

【题目】已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003molL﹣1s﹣1 . ,则6s时c(A)= molL﹣1 , C的物质的量为mol;若反应经一段时间后,达到平衡时A的转化率为 , 如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为;
(3)判断该反应是否达到平衡的依据为(填正确选项前的字母): a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为 .