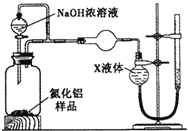
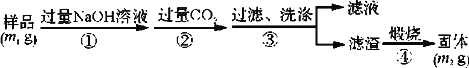题目内容
【题目】在常温常压下,24mLH2S和O2的混合气体点燃后,生成6mLSO2,则原混合气体中H2S的体积可能为
A. 10mLB. 12mLC. 16mLD. 18mL
【答案】B
【解析】
依据阿伏加德罗推论可知:恒温恒压下,![]() =
=![]() ;H2S和O2反应时有两种情况即当氧气过量时发生2H2S+3O2
;H2S和O2反应时有两种情况即当氧气过量时发生2H2S+3O2![]() 2H2O+2SO2、当氧气少量时会发生2H2S+O2
2H2O+2SO2、当氧气少量时会发生2H2S+O2![]() 2H2O+2S↓。据此解题。
2H2O+2S↓。据此解题。
设原混合气体中H2S的体积为x mL,则:
2H2S+3O2![]() 2H2O+2SO2
2H2O+2SO2
2Vm 3Vm 2Vm 2Vm
x y 6mL
计算可得
x=6mL y=9mL
所以反应生成SO2的H2S为 6mL。
当氧气过量时,气体总体积为24mL,所以H2S为6mL,O2为18mL;
当H2S过量时,H2S与O2反应的产物有SO2和S,其中生成SO2的H2S为 6mL,O2为9mL,生成S的H2S与O2总量为 24-6-9=9mL,涉及到的反应为:
2H2S+O2![]() 2H2O+2S↓,其中由于
2H2O+2S↓,其中由于![]() =
=![]() ,则
,则![]() =
=![]() =
=![]() 。因此H2S总体积为6+6=12mL,O2为9+3=12mL。
。因此H2S总体积为6+6=12mL,O2为9+3=12mL。
答案选B。

练习册系列答案
相关题目