题目内容
【题目】金属钼(![]() )在工业和国防建设中有重要的作用。钼的常见化合价为
)在工业和国防建设中有重要的作用。钼的常见化合价为![]() 。由钼精矿(主要成分是
。由钼精矿(主要成分是![]() )制备单质钼和钼酸钠晶体(
)制备单质钼和钼酸钠晶体(![]() ),部分流程如下图所示:
),部分流程如下图所示:
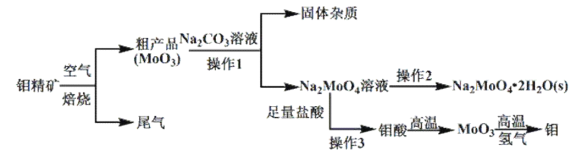
已知:钼酸微溶于水,可溶于碱溶液。
回答下列问题:
(1)钼精矿在空气中焙烧时,发生的主要方程式为_______________________。
(2)钼精矿焙烧时排放的尾气对环境会产生危害,请你提出一种实验室除去该尾气的方法________________________。
(3)操作2的名称为_________________________________。
(4)实验室由钼酸经高温制![]() ,所用到的硅酸盐材料仪器的名称是____________________________。
,所用到的硅酸盐材料仪器的名称是____________________________。
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中![]() 、
、![]() ,在结晶前需加入
,在结晶前需加入![]() 固体以除去溶液中的
固体以除去溶液中的![]() 。当
。当![]() 开始沉淀时,
开始沉淀时,![]() 的去除率是_________。[
的去除率是_________。[![]() 、
、![]() ,溶液体积变化可忽略不计]
,溶液体积变化可忽略不计]
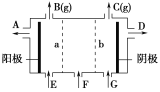
(6)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分数(![]() )。
)。
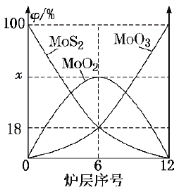
①![]() ___________。
___________。
②焙烧炉中也会发生![]() 与
与![]() 反应生成
反应生成![]() 和
和![]() ,还原剂为_________。若反应中转移
,还原剂为_________。若反应中转移![]() ,则消耗的还原剂的物质的量为______________。
,则消耗的还原剂的物质的量为______________。
【答案】![]() 可用氨水或氢氧化钠溶液吸收等其他合理答案 蒸发浓缩、冷却结晶、过滤、洗涤、干燥 坩埚 95.6% 64
可用氨水或氢氧化钠溶液吸收等其他合理答案 蒸发浓缩、冷却结晶、过滤、洗涤、干燥 坩埚 95.6% 64 ![]()
![]()
【解析】
根据流程图信息分析得:灼烧泪精矿,MoS2燃烧,反应方程式为2MoS2+7O2![]() 2MoO3+4SO2,碱性条件下,MoO3和Na2CO3溶液反应,反应方程式为MoO3+CO32-=MoO42-+CO2↑,溶液中的溶质为Na2MoO4,将溶液蒸发浓缩、冷却结晶,然后重结晶得到Na2MoO4·2H2O,Na2MoO4与足量盐酸反应生成钼酸,高温灼烧钼酸生成MoO3,.氢气还原MoO3得到Mo,以此解答该题。
2MoO3+4SO2,碱性条件下,MoO3和Na2CO3溶液反应,反应方程式为MoO3+CO32-=MoO42-+CO2↑,溶液中的溶质为Na2MoO4,将溶液蒸发浓缩、冷却结晶,然后重结晶得到Na2MoO4·2H2O,Na2MoO4与足量盐酸反应生成钼酸,高温灼烧钼酸生成MoO3,.氢气还原MoO3得到Mo,以此解答该题。
(1)根据流程图分析知,钼精矿焙烧时,反应方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(2)钮精矿焙烧时排放的尾气含有二氢化硫,会形成酸雨:二氢化硫为酸性氧化物,可用氨水或氢氢化钠溶液吸收,故答案为:可用氨水或氢氧化钠溶液吸收;
(3)操作2是从Na2MoO4溶液中获取Na2MoO4·2H2O晶体,操作是将溶液蒸发浓缩、冷却结晶,然后过滤、洗涤、干燥,故答案为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(4)高温灼烧钼酸生成MoO3,所用的硅酸盐材料仪器为坩埚,故答案为:坩埚;
(5)已知:![]() 、
、![]() ,
,![]() ,
,![]() ,当BaMoO4开始沉淀时,c(Ba2+)=
,当BaMoO4开始沉淀时,c(Ba2+)=![]() ,此时c(SO42-)=
,此时c(SO42-)=![]() ,则SO42-的去除率=
,则SO42-的去除率=![]() ,故答案为:95.6%;
,故答案为:95.6%;
(6)①由图2可知,6层中存在的固体物质分别为MoS2、MoO3、MoO2,图象分析MoS2、MoO3的物质的量百分比均为18%,根据Mo元素守恒,则MoO2的物质的量百分比为64%,则x为64;故答案为:64;
②MoS2与MoO3反应生成MoO2和SO2,反应为:![]() ,其中MoS2中Mo元素化合价不变,S元素由-2升高到+4价,被氧化,作还原剂;则转移12mol电子时,消耗的还原剂的物质的量为1mol,反应中转移
,其中MoS2中Mo元素化合价不变,S元素由-2升高到+4价,被氧化,作还原剂;则转移12mol电子时,消耗的还原剂的物质的量为1mol,反应中转移![]() ,消耗的还原剂的物质的量为0.25mol,故答案为:
,消耗的还原剂的物质的量为0.25mol,故答案为:![]() ;
;![]() 。
。