题目内容
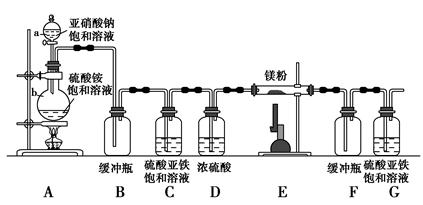
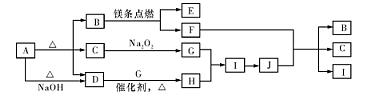
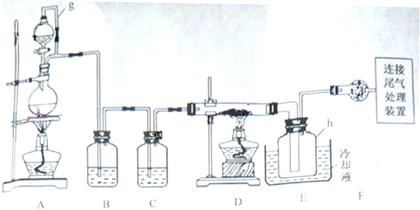
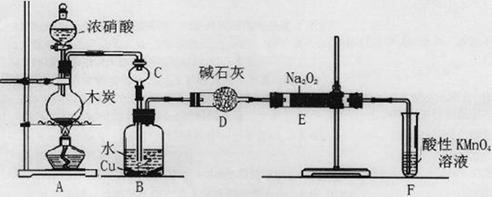
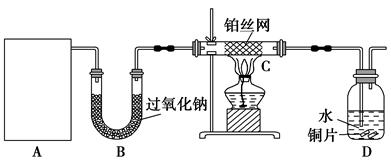
(12分)下图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下的气态化合物,C为常温下的液态化合物,图中有部分生成物未标出。
请填写以下空白:
(1)A的化学式为 ,B的电子式为 。
(2)写出下列反应的化学方程式:
D+G→H 。
F+J→B+C+I 。
(3)0.3 mol I与足量C反应转移电子的物质的量为 mol。
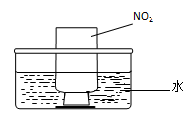
(4)容积为10 mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I与G的体积分别为 mL, mL。
请填写以下空白:

(1)A的化学式为 ,B的电子式为 。
(2)写出下列反应的化学方程式:
D+G→H 。
F+J→B+C+I 。
(3)0.3 mol I与足量C反应转移电子的物质的量为 mol。
(4)容积为10 mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I与G的体积分别为 mL, mL。
(1) NH4HCO3(2分), (2分)
(2分)
(2)4NH3+5O2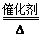 4NO+6H2O (2分) C+4HNO3(浓)
4NO+6H2O (2分) C+4HNO3(浓)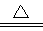 =CO2↑+4NO2↑+2H2O(2分)
=CO2↑+4NO2↑+2H2O(2分)
(3)0.2(2分)
(4)8(1分)2(1分)
 (2分)
(2分)(2)4NH3+5O2
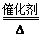 4NO+6H2O (2分) C+4HNO3(浓)
4NO+6H2O (2分) C+4HNO3(浓) =CO2↑+4NO2↑+2H2O(2分)
=CO2↑+4NO2↑+2H2O(2分)(3)0.2(2分)
(4)8(1分)2(1分)
试题分析:(1)已知A分解得到等物质的量的B、C、D,分析反应特点判断A是碳酸氢铵,化学式为NH4HCO3,镁条在B中燃烧,说明B是二氧化碳,则B的电子式为
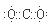 ;
;(2)铵盐与碱共热得D为氨气,过氧化钠与水反应生成G氧气,所以氨气与氧气的催化氧化反应的化学方程式为4NH3+5O2
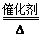 4NO+6H2O ;J为硝酸,F为碳单质,所以F+J→B+C+I的化学方程式为C+4HNO3(浓)
4NO+6H2O ;J为硝酸,F为碳单质,所以F+J→B+C+I的化学方程式为C+4HNO3(浓) =CO2↑+4NO2↑+2H2O(2分);
=CO2↑+4NO2↑+2H2O(2分);(3)I为NO2,与水的反应:3NO2+H2O=2HNO3+NO既作氧化剂又作还原剂,所以0.3mol的NO2与水的反应中转移电子的物质的量是0.2mol,
(4)NO2与O2恰好反应时物质的量之比是4:1,所以10mL混合气体中有8mL NO2,2mL O2

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



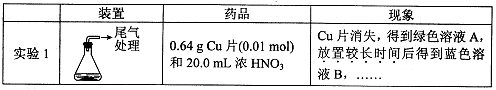
 Cu(NO2)42-(绿色)
Cu(NO2)42-(绿色)