题目内容
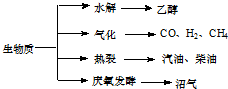
 生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.(1)由生物质能获得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及许多烃类物质.当两者1:1催化反应,其原子利用率达100%,合成的物质可能是
a.汽油 b.甲醇 c.甲醛 d.乙酸
(2)甲醇是一种重要的化工原料,工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ?mol-1.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
a.c1=c2 b.2Q1=Q3 c.K1=K3 d.α2+α3<100%
(3)在一定温度和压强下,CO和H2催化合成二甲醚的反应为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)

①若一体积可变的密闭容器中充入3mol H2、3mol CO、1mol CH3OCH3、1mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.则:反应开始时:v(正)>v(逆)的理由是:
平衡时,n(CH3OCH3)=
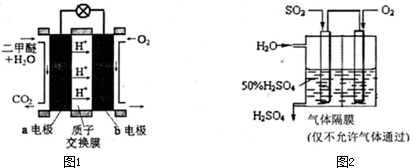
②右图为绿色电源“二甲醚燃料电池”的工作原理示意图.b电极是
(2)A.根据是否形成等效平衡解题;
B.增大压强平衡向体积减小的方向移动;
C.平衡常数只与温度有关;
D.无法求出转化率;
(3)①反应前后气体总质量不变;用差量法解题,方程式中3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)减少了4mol;
②负极失电子,正极得电子;(CH3)2O-12e-+3H2O=2CO2+12H+.
故答案为:cd;
(2)A.1molCO、2molH2与1mol CH3OH的等效的,平衡时CH3OH的浓度c1=c2,故A正确;
B.丙的反应物投入量是甲的二倍,容积相同,压强比甲大,平衡向右进行,放出的热量2Q1<Q3,故B错误;
C.平衡常数只与温度有关,温度相同,平衡常数相同,故C正确;
D.无法求出转化率,故D错误,
故答案为:ac;
(3)①反应前后气体总质量不变,同温、同压下,达到平衡时,气体密度增大,即气体体积缩小;平衡时混合气体密度是同温同压下起始时的1.6倍,则总物质的量变为原先的0.625倍,总物质的量=8×0.625=5mol,反应前后减少了3mol,设反应生成甲醚Xmol
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)减少了4mol,得
1 4
x 3
| 1 |
| x |
| 4 |
| 3 |
解得:x=0.75mol
平衡时,n(CH3OCH3)=1+0.75=1.75mol,
故答案为:反应前后气体总质量不变,同温、同压下,达到平衡时,气体密度增大,即气体体积缩小,平衡正移; 1.75;
②氧气得电子,化合价降低,故b电极是正极;由图知在a电极二甲醚与水反应生成二氧化碳和氢离子,故a电极的反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,
故答案为:正;(CH3)2O-12e-+3H2O=2CO2+12H+.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案(15分)生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如下图。
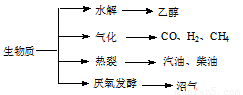
(1)下列有关说法正确的是 。
a.生物质能,本质上能量来源于太阳能
b.由纤维素水解获得的乙醇作燃料是利用了生物质能
c.生物质裂解获得的汽油、柴油等属于纯净物
d.由植物秸杆等厌氧发酵获得的沼气,主要成分是甲烷
(2)由生物质能获得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)甲醇是一种重要的化工原料,工业上合成甲醇的反应:
CO(g)+2H2(g) CH3OH(g) △H= -90.8kJ·mol-1。
CH3OH(g) △H= -90.8kJ·mol-1。
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
|
容器 |
甲 |
乙 |
丙 |
|
反应物投入量 |
1molCO 、2molH2 |
1mol CH3OH |
2molCO、4molH2 |
|
CH3OH的浓度(mol/L) |
c1 |
c2 |
c3 |
|
反应的能量变化 |
放出Q1 kJ |
吸收Q2 kJ |
放出Q3 kJ |
|
平衡常数 |
K1 |
K2 |
K3 |
|
反应物转化率 |
α 1 |
α 2 |
α 3 |
下列说法正确的是 。
a. c1 = c2 b. 2Q1 = Q3 c. K1=K3 d. α2+ α3< 100%
(4)在一定温度和压强下,CO和H2催化合成二甲醚的反应为:
3H2(g)+3CO(g)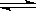 CH3OCH3(g)+CO2(g)
CH3OCH3(g)+CO2(g)
①若一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。则:①反应开始时正、逆反应速率的大小:v(正)____v(逆)(填“ >”、“ < ”或“=”),理由是
。平衡时n(CH3OCH3)= mol。
②下图为绿色电源“直接二甲醚燃料电池”的工作原理示意图。
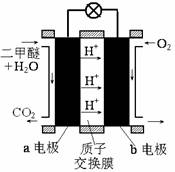
b电极是 极;a电极的反应式为 。