题目内容
【题目】如图所示为“铁链环”结构,图中两环相交部分A、B、C、D表示物质间的反应。下列对应部分反应的离子方程式书写不正确的是
![]()
A. C12+2OH-=Cl-+ClO-+2H2O
B. Cu2++2OH-=Cu(OH)2↓
C. SO42-+Ba2+=BaSO4↓
D. OH-+HCO3-=H2O+CO32-
【答案】B
【解析】
A.氯气与NaOH反应生成NaCl、NaClO、水,离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故A错误;
B.NaOH和硫酸铜反应生成氢氧化铜和硫酸钠,离子反应为Cu2++2OH-═Cu(OH)2↓,故B正确;
C.硫酸铜、氢氧化钡反应生成硫酸钡和氢氧化铜,离子反应为Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓,故C错误;
D.氢氧化钡与碳酸氢钠反应生成碳酸钡、水,若碳酸氢钠少量,离子方程式为HCO3-+Ba2++OH-═BaCO3↓+H2O,若碳酸氢钠足量,离子方程式为2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32-,故D错误;
正确答案:B。

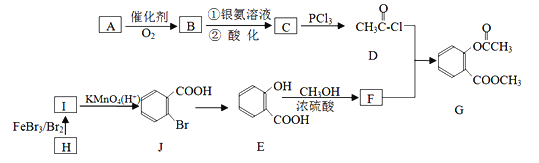
【题目】下图是某化学兴趣小组设计的利用电子垃圾(含70% Cu、25% Al、4% Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:

已知下列信息:Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
开始沉淀 | 1.1 | 4.0 | 5.4 |
完全沉淀 | 3.2 | 5.2 | 6.7 |
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式:_________________________________。
(2)在操作Ⅱ中,x的取值范围是____________。
(3)在操作Ⅲ中,蒸发浓缩需要的玻璃仪器有________________。
(4)由滤渣a制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
甲:滤渣a―→H2SO4―→操作Ⅲ―→Al2(SO4)3·18H2O
乙:滤渣a―→H2SO4―→适量Al粉,过滤―→操作Ⅲ―→Al2(SO4)3·18H2O
丙:滤渣a―→NaOH溶液,过滤―→H2SO4―→操作Ⅲ―→Al2(SO4)3·18H2O
综合考虑上述三种方案,最具可行性的是______(填序号)。
(5)为测定CuSO4·5H2O晶体的纯度,进行下列实验:取a g 试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用b mol·L-1 EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-===CuY2-+2H+),滴定至终点,平均消耗EDTA溶液12.00 mL(常温时,5%的Na2H2Y水溶液,其pH为4~6),则CuSO4·5H2O晶体的纯度是________________。
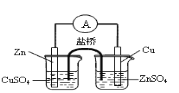
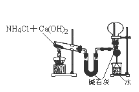
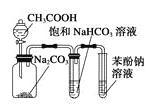
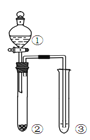
【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D