题目内容
13.用括号内试剂和方法除去下列各物质中的少量杂质,正确的是( )| A. | 苯中的甲苯(酸性高锰酸钾溶液溶液,分液) | |
| B. | 乙烷中的乙烯(酸性高锰酸钾溶液,洗气) | |
| C. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液,分液) | |
| D. | 苯中的苯酚(浓Br2水,过滤) |
分析 A.甲苯被高锰酸钾氧化后与苯不分层;
B.乙烯被高锰酸钾氧化生成二氧化碳;
C.乙酸与碳酸钠反应后,与乙酸乙酯分层;
D.溴、三溴苯酚均易溶于苯.
解答 解:A.甲苯被高锰酸钾氧化后与苯不分层,不能分液分离,故A错误;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,不能除杂,应选溴水、洗气除杂,故B错误;
C.乙酸与碳酸钠反应后,与乙酸乙酯分层,然后分液可除杂,故C正确;
D.溴、三溴苯酚均易溶于苯,不能除杂,应选NaOH、分液,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及除杂原则为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
3.下列气体在氧气中充分燃烧后,其产物既可使无水硫酸铜变蓝,又可使澄清石灰水变浑浊的是( )
| A. | H2S | B. | CH4 | C. | H2 | D. | CO |
4.2g NaOH固体溶于水配成250mL溶液取出其中50mL,则这50mL NaOH溶液中溶质的物质的量浓度为( )
| A. | 0.04 mol/L | B. | 0.2 mol/L | C. | 1 mol/L | D. | 2 mol/L |
1.化学小组测定一定质量的某镁铝混合物中镁的质量分数,设计了如下实验方案:
方案Ⅰ:镁铝混合物$→_{充分反应}^{足量溶液A}$测定生成气体的体积
方案Ⅱ:镁铝混合物$→_{充分反应}^{足量溶液B}$测定剩余固体的质量
下列有关判断中不正确的是( )
方案Ⅰ:镁铝混合物$→_{充分反应}^{足量溶液A}$测定生成气体的体积
方案Ⅱ:镁铝混合物$→_{充分反应}^{足量溶液B}$测定剩余固体的质量
下列有关判断中不正确的是( )
| A. | 溶液A选用NaOH溶液 | |
| B. | 若溶液B选用浓硝酸,则测得镁的质量分数偏小 | |
| C. | 溶液A和B均可选用稀硝酸 | |
| D. | 实验室中方案Ⅱ更便于实施 |
8.以下表示正确的是( )
| A. | 明矾净水原理:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 醋酸溶于水电离:CH3COOH?CH3COO-+H+ | |
| C. | 碳酸钠溶液水解:CO32-+H2O═HCO3-+OH- | |
| D. | 硫酸钡溶解于水中:BaSO4?Ba2++SO42- |
18.今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A. | ③、④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 | |
| B. | ②、③两溶液等体积混合,所得溶液中c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 分别加水稀释10倍,四种溶液的pH ①>②>④>③ | |
| D. | VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va:Vb=11:9 |
5.苯和浓硝酸、浓硫酸混和后在100-110℃时发生反应的生成物是( )
| A. | 硝基苯 | B. | 对二硝基苯 | C. | 间二硝基苯 | D. | 三硝基苯 |
2.对于可逆H2(g)+I2(g)$\stackrel{△}{?}$2HI(g),下列情况一定能说明反应已达到平衡状态的是( )
| A. | 气体总压强不再随时间而改变时 | |
| B. | 气体的总质量不再改变时 | |
| C. | 混合气体中各组成成分的含量不再改变时 | |
| D. | 单位时间内每消耗1 mol I2,同时有2 mol HI生成时 |
3.对达到平衡状态的可逆反应:A+B?C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是( )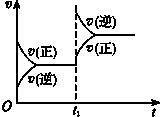

| A. | A、B都是气体,C、D都不是气体 | B. | A、B都是气体,C、D有一种是气体 | ||
| C. | C、D都是气体,A、B都是气体 | D. | C、D都是气体,A、B有一种是气体 |