题目内容
11.现欲配制480mL 0.1mol/L的Na2S2O3溶液.(1)需要量取25.0mL 2.0mol/L的Na2S2O3溶液;
(2)下列操作造成配制出的Na2S2O3溶液浓度偏低的是②④.
①量取2.0mol/L的Na2S2O3溶液时,仰视刻度线
②未洗涤烧杯和玻璃棒
③定容时,俯视刻度线
④定容后摇匀发现液面低于刻度线,继续滴加蒸馏水至刻度线.
分析 (1)依据配制溶液的体积选择合适的容量瓶,依据溶液稀释过程中所含溶质的物质的量不变计算需要浓溶液体积;
(2)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)欲配制480mL 0.1mol/L的Na2S2O3溶液,应选择500mL容量瓶,设需要浓溶液体积为V,则依据溶液稀释过程中所含溶质的物质的量不变得:V×2.0mol/L=0.1mol/L×0.5L,解得V=0.0250L;
故答案为:25.0;
(2)①量取2.0mol/L的Na2S2O3溶液时,仰视刻度线,导致浓溶液体积偏大,量取的溶质的物质的量偏大,溶液浓度偏高,故不选;
②未洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故选;
③定容时,俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故不选;
④定容后摇匀发现液面低于刻度线,继续滴加蒸馏水至刻度线,导致溶液体积偏大,溶液浓度偏低,故选;
故选:②④.
点评 本题考查了一定物质的量浓度溶液的配制及误差分析,明确配制原理和容量瓶规格的选择是解题关键,题目难度不大.

练习册系列答案
相关题目
6.下列物质在生活中应用时,起还原作用的是( )
| A. | 食醋除水垢 | B. | 硅胶作干燥剂 | ||
| C. | 漂白粉漂白织物 | D. | 铁粉作食品袋内的脱氧剂 |
16.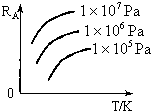 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )
 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )| A. | 正反应吸热,m+n>x+y | B. | 正反应吸热,m+n<x+y | ||
| C. | 正反应放热,m+n>x+y | D. | 正反应放热,m+n<x+y |
3.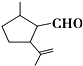 有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
 有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )| A. | 先加KMnO4酸性溶液,再加银氨溶液,微热 | |
| B. | 先加溴水,再加KMnO4酸性溶液 | |
| C. | 先加银氨溶液,微热,再加溴水 | |
| D. | 先加入足量的新制Cu(OH)2悬浊液,微热,酸化后再加溴水 |
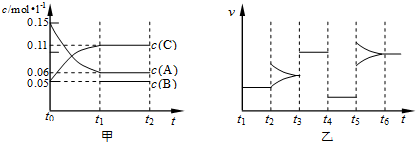
 2C(g)+B(g)△H=+150akJ/mol.
2C(g)+B(g)△H=+150akJ/mol.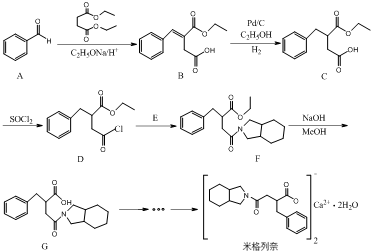
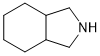 .
.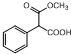 )为C的同系物,写出符合下列条件的X的一种同分异构体的结构简式:
)为C的同系物,写出符合下列条件的X的一种同分异构体的结构简式: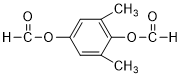 或
或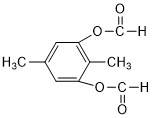 或
或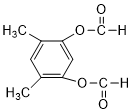 (以上一种即可).
(以上一种即可).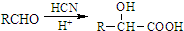 ②
②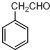 为原料制备
为原料制备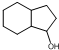 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: