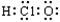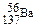题目内容
W、X、Y、Z是原子序数依次增大的同一周期元素,原子序数均小于18,W、X是金属元素,Y、Z是非金属元素。
(1)已知:W、X各自的氧化物对应的水化物可以反应生成盐和水,写出X的氧化物与过量氢氧化钠溶液反应的离子方程式 。
(2)W与Y可形成化合物W2Y,该化合物水溶液呈碱性,用离子方程式解释其原因:
。
(3)Y的某氧化物通入Z单质的水溶液中,发生反应生成两种强酸的化学方程式为:
。
(4)写出Z-离子的核外电子排布式: 。
(5)W、X、Y、Z四种元素简单离子的半径由小到大的顺序是
< < < (写离子符号)。
(1)已知:W、X各自的氧化物对应的水化物可以反应生成盐和水,写出X的氧化物与过量氢氧化钠溶液反应的离子方程式 。
(2)W与Y可形成化合物W2Y,该化合物水溶液呈碱性,用离子方程式解释其原因:
。
(3)Y的某氧化物通入Z单质的水溶液中,发生反应生成两种强酸的化学方程式为:
。
(4)写出Z-离子的核外电子排布式: 。
(5)W、X、Y、Z四种元素简单离子的半径由小到大的顺序是
< < < (写离子符号)。
20.(13分)
(1)Al2O3+2OH-==2AlO2+H2O(2分)
(2)S2-+H2O HS-+OH-(2分)
HS-+OH-(2分)
(3)SO2+Cl2+2H2O==H2SO4+2HCl(3分)
(4)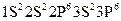 (3分)
(3分)
(5)Al3+<Na+<Cl-<S2-(3分)
(1)Al2O3+2OH-==2AlO2+H2O(2分)
(2)S2-+H2O
 HS-+OH-(2分)
HS-+OH-(2分)(3)SO2+Cl2+2H2O==H2SO4+2HCl(3分)
(4)
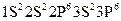 (3分)
(3分)(5)Al3+<Na+<Cl-<S2-(3分)
略

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
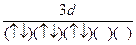
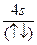
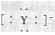 ,则原子序数:Y>Z>X
,则原子序数:Y>Z>X