题目内容
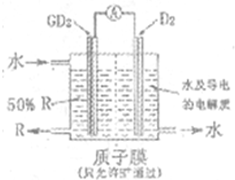
A、B、C是三种短周期元素的单质,甲、乙是两种常见的化合物,这些单质、化合物之间存在如下图所示关系(反应条件均未注明).回答下列问题:
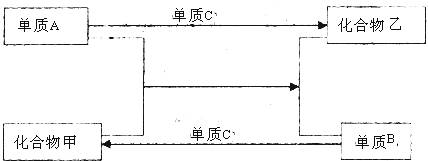
下列(1)~(3)中的A不在同一主族。
(1)若A为ⅢA族元素,则A是 ,B是 ,C是 。
(2)若化合物乙为氧化物,则单质A与化合物甲反应的化学方程式为:
。
(3)若化合物甲在常温,常压下为液态,则单质A与化合物甲反应的化学方程式为:
。
(1)Al H2 Cl2
(2)2 Mg+CO2![]() C+2MgO或C+H2O
C+2MgO或C+H2O![]() CO+H2或2C+SiO2
CO+H2或2C+SiO2![]() Si+2CO
Si+2CO
(3)2F2+2H2O=4HF+O2(C+H2O![]() CO+H2)
CO+H2)

 名校课堂系列答案
名校课堂系列答案现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B元素原子的核外p电子总数比s电子总数少1 |
| C原子p轨道上成对电子数等于未成对电子数,且与A同周期 |
| D元素的族序数与周期数的差为4,且不与A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(1)A的基态原子最外层有 种不同运动状态的电子,F位于 区。
(2)E2+的基态核外电子排布式为 ,AD4为 (填极性或非极性)分子。
(3)A、B、C三种元素的电负性由小到大的顺序是 (用元素符号表示),B和C两元素中,B的第一电离能较大的原因是 ,与AC2互为等电子体的分子的名称为 。(只写一种)
(4)BD3 中心原子的杂化方式为 ,其分子空间构型为 。
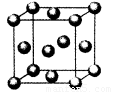
(5)用晶体的x射线衍射法对F的测定得到以下结果:F的晶胞为
面心立方最密堆积(如右图),又知该晶体的密度为ρg/cm3,
晶胞中该原子的配位数为 ;F的原子半径是 pm;
(阿伏加德罗常数为NA)。