题目内容
【题目】已知A、B、C三种元素的原子中,质于数:A<B<C,且都小于18。A元素原子的最外层电子数是次外层电子数的2倍;B元素原子的M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多1。试回答下列问题。
(1)写出三种元素的名称和符号:A______,B______,C______。
(2)画出三种元素的原子结构示意图:A______,B______,C______。
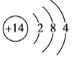
【答案】碳C 硅Si 氯Cl 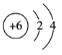
【解析】
A元素的原子最外层电子数是次外层电子数的2倍,则A原子核外电子排布为2、4,A是C元素;B元素的原子核外M层电子数是L层电子数的一半,则B原子核外电子排布为2、8、4,B为Si元素;C元素的原子次外层电子数比最外层电子数多1个,且原子序数大于B小于18,所以C原子核外电子排布为2、8、7,C是Cl元素,据此答题。
根据上述分析可知A是C元素,B是Si元素,C是Cl元素。
(1)A为碳元素,元素符号为C;B为硅元素,元素符号为Si;C为氯元素,元素符号为Cl;
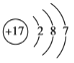
(2)碳原子的结构示意图为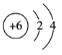 ,硅原子的结构示意图为
,硅原子的结构示意图为 ,氯原子的结构示意图为
,氯原子的结构示意图为 。
。

【题目】已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 地壳中含量最多的元素 |
Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
R | 核电荷数是Y与Q的核电荷数之和 |
E | N能层上只有一个电子,K、L、M层均排满电子 |
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图:___________。X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为______。
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)_____。
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)______,原因是________。
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:_____。
(5)R的一种配合物的化学式为RCl36H2O。已知0.01mol RCl36H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀。此配合物最可能是____。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2H2O
C.[R(H2O)4Cl2]Cl2H2O D.[R(H2O)3Cl3]3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:__,继续滴加氨水至过量,沉淀溶解,得到深蓝色溶液,写出反应的离子方程式为:__。