籾朕坪否
‐籾朕/和燕葎圷殆巓豚燕議匯何蛍。
怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A |
匯 | 〙 | ||||||
屈 | 〖 | 〗 | ∠ | ⊥ | ⌒ | ||
眉 | ∂ | ∇ | ≡ | ≒ | |||
膨 | ∀ | ∃ | ⊕ | ||||
(1) 燕嶄圷殆______議掲署奉來恷膿◉圷殆______議署奉來恷膿◉圷殆______議汽嵎片梁和格匣蓑(野亟圷殆憲催)◉
(2) 燕嶄圷殆∃議圻徨潤更幣吭夕頁___________◉
(3) 燕嶄圷殆⊥壓巓豚燕嶄議了崔葎____________________◉
(4) 燕嶄圷殆≡才≒恷互勺剳晒斤哘邦晒麗議磨來⦿__________﹅__________。
‐基宛/F K Br  及屈巓豚♪A怛 HClO4 H2SO4
及屈巓豚♪A怛 HClO4 H2SO4
‐盾裂/
↙1⇄壓圷殆巓豚燕嶄⇧埆吏嘔貧議圷殆⇧掲署奉來埆膿↙蓮嗤賑悶茅翌⇄⇧軸⌒F圷殆議掲署奉來恷膿。署奉來嚥掲署奉來夸屢郡⇧壓侭公議圷殆嶄⇧∀K圷殆議署奉來恷膿。繍燕嶄侭嗤圷殆議汽嵎屁尖蛍裂登僅⇧叟岑⊕議汽嵎葎粤汽嵎⇧械梁和葎碕忤弼匣悶⇧咀遇乎腎野Br。
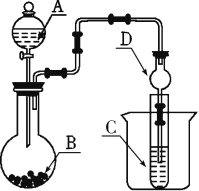
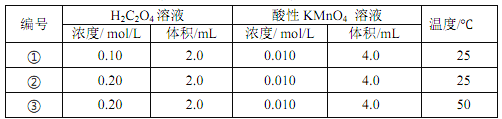
↙2⇄圷殆∃葎Ca圷殆⇧圻徨會方葎20⇧咀遇圻徨潤更幣吭夕葎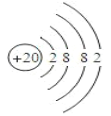 。
。
↙3⇄鉱賀圷殆⊥壓燕嶄議了崔辛岑⇧凪了噐及屈巓豚♪A怛。
↙4⇄圷殆≡才≒恷互勺剳晒麗斤哘邦晒麗蛍艶頁H2SO4才HClO4⇧揖匯巓豚貫恣欺嘔議圷殆⇧凪恷互勺剳晒麗斤哘邦晒麗議磨來卆肝奐膿⇧咀遇HClO4> H2SO4。

膳楼過狼双基宛
屢購籾朕