题目内容
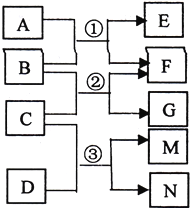
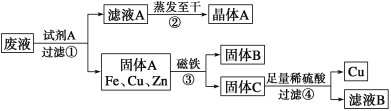
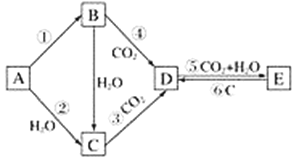
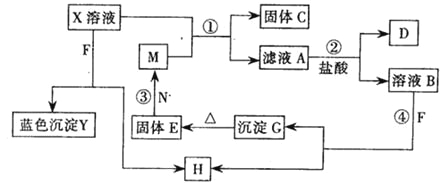
【题目】已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如下图,(部分反应产物已略去).
请回答下列问题;
(1)E的化学式为_____________________
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:_______________________
(3)在反应①②③④中属于置换反应的是_________________(填序号).
(4)反应②的离子方程式为___________________________________
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1. 6g.请回答下列问题:
①写出电解时的阳极反应式_______________________
②电解后溶液的pH为________________________假设电解前后溶液体积不变)
【答案】Fe2O3 铁丝上附有红色物质,溶液颜色逐渐变为浅绿色 ①③ 3Fe2++NO3-+4H+= 3Fe3++NO ↑ +2H2O 4OH--4e-=O2↑ +2H2O 1
【解析】
由题意:X为中学化学中一种常见的盐,F为淡黄色固体,与X溶液反应生成蓝色沉淀Y为氢氧化铜可知,F为Na2O2;X溶液中含铜离子;M、N为常见的金属,结合N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器,E和N反应生成M可知发生了置换反应,判断N为Al,E为Fe2O3;M为Fe,结合M和含铜离子的X溶液反应生成固体C为铜,滤液A为亚铁盐溶液,加入盐酸会发生反应生成无色气体D,说明A只能是硝酸亚铁,即X溶液为硝酸铜溶液;F为过氧化钠加入到溶液B中生成H为气体单质氧气,D为无色气体一氧化氮,D在空气中会出现红棕色二氧化氮。
(1)由分析可知E为:Fe2O3;
(2)将M丝插入盛有X溶液的试管中,是Fe和硝酸铜溶液反应生成铜和硝酸亚铁,反应一段时间后的现象:铁丝上附有红色物质,溶液颜色逐渐变为浅绿色;
(3)反应①是铁和硝酸铜溶液反应发生置换反应;②是硝酸亚铁和盐酸发生氧化还原反应;③是氧化铝和铁反应生成铝和氧化铁,是置换反应;④是硝酸铁和过氧化钠反应,不是置换反应,所以中属于置换反应的是①③;
(4)反应②是亚铁离子在硝酸溶液中发生的氧化还原反应,离子方程式为:反应②的离子方程式反应为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(5)①阳极电极反应是氢氧根离子放电,电极反应为:4OH--4e-=O2↑+2H2O;
②阳极电极反应为4OH--4e-=O2↑+2H2O;阴极电极反应为:Cu2++2e-=Cu;析出铜0.025mol,电子转移为0.05mol,由电极方程式可知生成氢离子0.05mol,则生成c(H+)=0.05mol÷0.5L=0.1mol·L-1,pH=1。

 阅读快车系列答案
阅读快车系列答案【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【题目】下图是某儿童微量元素体检报告单的部分数据,根据数据,回答下列问题:
北京市医疗机构临床检验结果报告单 | ||||
分析项目 | 检测结果 | 单位 | 参考范围 | |
1 | 锌(Zn) | 115.92 |
| 66~120 |
2 | 铁(Fe) | 6.95↓ |
| 7.52~11.82 |
3 | 钙(Ca) | 1.68 |
| 1.55~2.10 |
(1)该儿童体内_________元素含量偏低。
(2)报告单中“μmol·L-1”是__________(填“质量”“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的________性。
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是_______________________。
(5)取补血剂片用研钵研细,加入过量稀硫酸,取澄清液,然后滴加KSCN溶液,若溶液变为红色,则溶液中含有________(填离子符号),说明补血剂是否变质____________。