题目内容
查阅资料发现,金属钠不仅能与氧气和水反应,还能与很多种其他物质发生反应,其中包括与酒精在常温下反应,要研究金属钠和酒精、金属钠和水反应的异同点,下列的研究方法中用不到的是( )
| A.观察法 | B.分类法 | C.实验法 | D.比较法 |
B
试题分析:研究金属钠和酒精、金属钠和水反应的异同点,可以采用的研究方法有观察法,即观察两者发生反应的剧烈情况; 实验法和比较法,即通过实验比较两者反应的剧烈情况,分类法对研究金属钠和酒精、金属钠和水反应的异同点没有意义,故本题的答案选择B。
点评:本题考查了化学探究过程中所采用的研究方法,所以对学生科研基本功的考查,该题比较简单。

练习册系列答案
相关题目
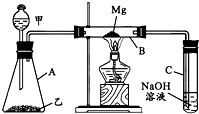
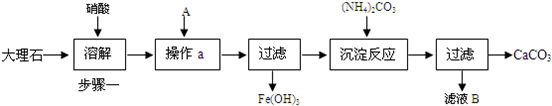
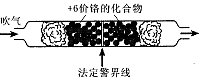
 Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。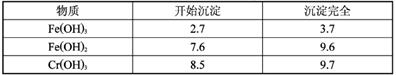
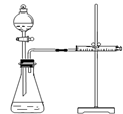
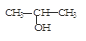 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2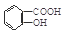 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备