题目内容
【题目】液体锌二次电池具有电压高、成本低、安全性强和可循环使用等特点。已知:①Zn(OH)2+2OH-=Zn(OH)![]() ;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
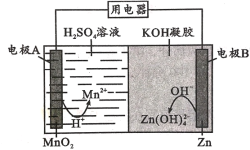
A.电池放电时,电子由电极B经导线流向电极A
B.电池反应为MnO2+ Zn + 4H++4OH-=Mn2+ + Zn(OH)![]() +2 H2 O
+2 H2 O
C.电池充电时,H+向电极A移动
D.电池充电时,电极B的质量增大
【答案】C
【解析】
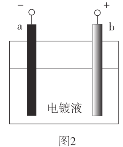
由图中信息可知,电极A上发生还原反应,电极B上发生氧化反应,则A为正极、B为负极。
A. 电池放电时,电子由负极经外电路流向正极,即由电极B经导线流向电极A,A说法正确;
B. 由图中两电极的物质转化关系可知,电池反应为MnO2+ Zn + 4H++4OH-=Mn2+ + Zn(OH)![]() +2 H2 O,B说法正确;
+2 H2 O,B说法正确;
C. 电池放电时,K+向正极迁移,即向电极A迁移;电池充电时,电极A变为阳极,电极反应式为Mn2+ +2 H2 O -2e- = MnO2+ 4H+;电极B变为阴极,电极反应式为Zn(OH)![]() + 2e+= Zn +4OH-,K+向阴极迁移,即向电极B移动,H+不可能向电极A移动,C说法错误;
+ 2e+= Zn +4OH-,K+向阴极迁移,即向电极B移动,H+不可能向电极A移动,C说法错误;
D. 电池充电时,电极B变为阴极,电极反应式为Zn(OH)![]() + 2e+= Zn +4OH-,电极B的质量增大,D说法正确。
+ 2e+= Zn +4OH-,电极B的质量增大,D说法正确。
本题选C。

练习册系列答案
相关题目