题目内容
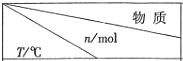
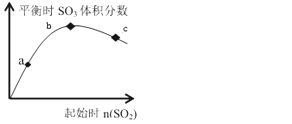
【题目】在一定温度下,只改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g)的影响如图所示,下列说法正确的是( )
A. 反应a、b、c点均为平衡点,且b点时SO2的转化率最高
B. b点时SO2与O2 的物质的之比约为2:1
C. a、b、c 三点平衡常数: Kb>Kc>Ka
D. a、b、c 三点反应速率大小为: vb>vc>va
【答案】B
【解析】
分析图像我们可知,在一定范围内,随着二氧化硫起始浓度的提高,平衡时三氧化硫的体积分数也会随之提高,但是当二氧化硫的起始浓度超过一定限度后,平衡时三氧化硫的体积会随着其增大而减小。
A.曲线上的点为平衡状态,当氧气的量一定时,二氧化硫的起始量越少,则二氧化硫的转化率越大,a点时SO2的转化率最大,故A错误;
B.由2SO2(g)+O2(g)2SO3(g)可知,b点时SO2与O2的物质的量之比约为2:1,SO3的体积分数最大,故B正确;
C.温度不变,则平衡常数不变,a、b、c三点平衡常数:Kb=Kc=Ka,故C错误;
D.浓度越大,反应速率越快,则a、b、c三点反应速率大小为:vc>vb>va,故D错误;
故选B。

 智慧小复习系列答案
智慧小复习系列答案【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
⑨ | ⑩ |
请回答下列问题:
(1)表中⑨号属于______区元素。
(2)③和⑧形成的一种常见溶剂,其分子立体空间构型为________。
(3)元素①和⑥形成的最简单分子X属于________分子(填“极性”或“非极性”)
(4)元素⑥的第一电离能________元素⑦的第一电离能;元素②的电负性________元素④的电负性(选填“>”、“=”或“<”)。
(5)元素⑨的基态原子核外价电子排布式是________。
(6)元素⑧和④形成的化合物的电子式为________。
(7)某些不同族元素的性质也有一定的相似性,如表中元素⑩与元素⑤的氢氧化物有相似的性质。请写出元素⑩的氢氧化物与NaOH溶液反应的化学方程式:____________________。
【题目】近年来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.
![]() 活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入
活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入![]() NO和
NO和![]() 固体活性炭
固体活性炭![]() 无杂质
无杂质![]() ,生成气体E和气体
,生成气体E和气体![]() 当温度分别在
当温度分别在![]() 和
和![]() 时,测得平衡时各物质的物质的量如下表:
时,测得平衡时各物质的物质的量如下表:
| 活性炭 | NO | E | F |
|
|
|
|
|
|
|
|
|
|
![]() 结合上表数据,写出NO与活性炭反应的化学方程式 ______ ;
结合上表数据,写出NO与活性炭反应的化学方程式 ______ ;
![]() 上述反应的平衡常数表达式
上述反应的平衡常数表达式![]() ______ ,根据上述信息判断,
______ ,根据上述信息判断,![]() 和
和![]() 的关系是 ______ ;
的关系是 ______ ;
A.![]() B.
B.![]() C.无法比较
C.无法比较
![]() 在
在![]() 下反应达到平衡后,下列措施能改变NO的转化率的是 ______ ;
下反应达到平衡后,下列措施能改变NO的转化率的是 ______ ;
![]() 增大
增大![]()
![]() 增大压强
增大压强![]() 升高温度
升高温度![]() 移去部分F
移去部分F
![]() 碘循环工艺不仅能吸收
碘循环工艺不仅能吸收![]() 降低环境污染,同时又能制得
降低环境污染,同时又能制得![]() ,具体流程如图所示
,具体流程如图所示

![]() 用离子方程式表示反应器中发生的反应 ______ ;
用离子方程式表示反应器中发生的反应 ______ ;
![]() 用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出
用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出![]() 的目的是 ______ ;
的目的是 ______ ;
![]() 开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池
开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池![]() 简称
简称![]() 由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示
由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示
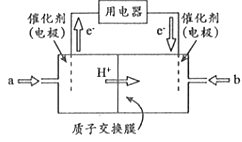
通过a气体的电极是原电池的 ______ 极![]() 填“正”或“负”
填“正”或“负”![]() ,b电极反应式为 ______ .
,b电极反应式为 ______ .