题目内容
标准状态下,在四个干燥的烧瓶中分别充入:① 纯净的氨气,② 混有1/3体积空气的氯化氢气体,③ 纯净的NO2气体,④ 混有少量O2的NO2气体。然后各做喷泉实验。实验后,三烧瓶中溶液的物质的量浓度大小关系是
| A.①=②=③=④ | B.①=②=③>④ | C.①=②=③<④ | D.④>①=②>③ |
B
解析试题分析:气体的体积相等,相同条件下气体的物质的量相等,令气体的物质的量为3mol,则烧瓶的容积为3×22.4L。再判断烧瓶中溶液的体积、溶质的物质的量,再根据物质的量浓度公式判断浓度比。
①纯净的氨气,完全溶于水,溶液的体积等于烧瓶容积,所以溶液浓度为 ;②混有1/3体积空气的氯化氢气体,氯化氢为1mol,溶液体积等于烧瓶容积的1/3,所以溶液物质的量浓度为
;②混有1/3体积空气的氯化氢气体,氯化氢为1mol,溶液体积等于烧瓶容积的1/3,所以溶液物质的量浓度为 ;③纯净的NO2气体,发生反应3NO2+H2O=2HNO3+NO,生成硝酸2mol,1molNO,所以溶液体积等于烧瓶容积的2/3,所以溶液的物质的量浓度为
;③纯净的NO2气体,发生反应3NO2+H2O=2HNO3+NO,生成硝酸2mol,1molNO,所以溶液体积等于烧瓶容积的2/3,所以溶液的物质的量浓度为 ;④混有少量O2的NO2气体,把NO2分成两部分:第一部分:4NO2+O2+2H2O=4HNO3,由于O2很少,故还有:第二部分:3NO2+H2O=2HNO3+NO.这样第一部分反应中,5份的气体(4NO2+O2)生成4份HNO3,这部分溶液体积等于二氧化氮与氧气的体积,故这部分的浓度为
;④混有少量O2的NO2气体,把NO2分成两部分:第一部分:4NO2+O2+2H2O=4HNO3,由于O2很少,故还有:第二部分:3NO2+H2O=2HNO3+NO.这样第一部分反应中,5份的气体(4NO2+O2)生成4份HNO3,这部分溶液体积等于二氧化氮与氧气的体积,故这部分的浓度为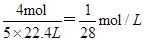 。第二部分浓度为=
。第二部分浓度为= ,所以比只有NO2气体形成的溶液浓度小,故溶液浓度①=②=③>④,答案选B。
,所以比只有NO2气体形成的溶液浓度小,故溶液浓度①=②=③>④,答案选B。
考点:考查喷泉实验中有关物质的量浓度计算
点评:该题是中等难度的试题,试题综合性强,侧重对学生能力的培养。该题的 关键是明确喷泉实验原理、物质的量浓度的计算依据,然后结合题意灵活运用即可。难点是选项④,注意④中把整体分为两部分考虑,关键是判断溶液体积与气体的体积关系。

 阅读快车系列答案
阅读快车系列答案常温下,下列说法正确的是
| A.往CH3COOH溶液中加水,c(OHˉ)和c(H+)均增大 |
| B.物质的量浓度均为0.1mol?Lˉ1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)>c(CH3COOˉ) |
| C.某浓度的氯化铵溶液中存在c(NH4+)>c(Clˉ)>c(H+)> c(OHˉ) |
| D.在pH=4的氯化铵溶液中c(H+)+ c(NH4+)=" c(Clˉ)+" c(OHˉ) |
室温下,某浓度的醋酸溶液中n(CH3COO-)=0.01mol,下列叙述正确的是
| A.向该醋酸溶液中加入等体积等浓度的盐酸,抑制醋酸的电离,溶液中c(H+)增大 |
| B.若醋酸溶液体积为1L,则c(CH3COOH)=0.01mol/L |
| C.与NaOH恰好中和时,溶液中c(Na+)<c(CH3COO-) |
| D.与等体积等浓度的醋酸钠溶液混合,溶液中c(Na+)+ c(H+)=c(CH3COO-)+ c(OH-) |
下列说法正确的是
A.已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH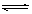 CH3COO-+H+,加少量烧碱溶液可使溶液中 CH3COO-+H+,加少量烧碱溶液可使溶液中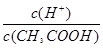 值增大。 值增大。 |
B.25℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O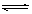 H++OH-逆向移动,c(H+)降低 H++OH-逆向移动,c(H+)降低 |
| C.取c(H+)="0.01" mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3-) |
室温下,向amo1·L-1氨水中逐滴加入盐酸,下列描述不正确的是
| A.溶液的pH减小 |
B.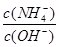 增大 增大 |
| C.水的电离程度先减小后增大 |
D.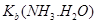 不变 不变 |
室温下向10 mL pH = 3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
| B.溶液中C(CH3COO-)/C(CH3COOH).c(OH-)不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH = 11的NaOH溶液,混合液pH=7 |
下列说法中错误的是
| A.0.5 L 2 mol·L-1 AlCl3溶液中,Al3+和Cl-总数小于4×6.02×1023个 |
| B.制成0.5 L 10 mol·L-1的盐酸,需要标准状况下的氯化氢气体112 L |
| C.从1 L 1 mol·L-1的NaCl溶液中移取出10 mL溶液,其浓度是1 mol·L-1 |
| D.10 g 98%的硫酸(密度为1.84 g·cm-3)与10 mL18.4 mol·L-1的硫酸的浓度不同 |