题目内容
7.NA表示阿伏加德罗常数的值.下列说法不正确的是( )| A. | 0.5mol H2O中含有的原子总数为1.5 NA | |
| B. | 0.2mol O2 所占有的体积为4.48L | |
| C. | 22g 二氧化碳气体中所含有的分子数目为0.5 NA | |
| D. | 100mL2mol/L的Na2CO3溶液中含有的Na+数目为0.4NA |
分析 A、水为三原子分子;
B、氧气所处的状态不明确;
C、分子个数N=$\frac{m}{M}{N}_{A}$;
D、求出碳酸钠的物质的量,然后根据1mol碳酸钠中含2mol钠离子来分析.
解答 解:A、水为三原子分子,故0.5mol水中含1.5mol原子即1.5NA个,故A正确;
B、氧气所处的状态不明确,故0.2mol氧气的体积不明确,故B错误;
C、22g二氧化碳中的分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{22g}{44g/mol}{N}_{A}$=0.5NA个,故C正确;
D、溶液中的碳酸钠的物质的量n=CV=2mol/L×0.1L=0.2mol,而1mol碳酸钠中含2mol钠离子,故0.2mol碳酸钠中含0.4mol钠离子即0.4NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
18.下列关于钢铁腐蚀的叙述正确的是( )
| A. | 钢铁插入水中,水下部分比空气与水交界处更容易腐蚀 | |
| B. | 钢铁在海水中比在河水中更易腐蚀,主要是由于海水中有大量电解质 | |
| C. | 钢铁设备上连接铜块可以防止钢铁腐蚀 | |
| D. | 钢铁设备与外加直流电源的正极相连可以防止钢铁腐蚀 |
15.下列说法正确的是( )
①最外层电子数是2的元素一定是金属元素
②元素周期表中,非金属性最强的元素是F
③盐酸是强酸,H2S是弱酸,故非金属性:Cl>S
④X元素的阳离子和Y元素的阴离子具有相同的电子层结构,则原子序数:X>Y
⑤O2和O3属于同素异形体,故它们的性质相同.
①最外层电子数是2的元素一定是金属元素
②元素周期表中,非金属性最强的元素是F
③盐酸是强酸,H2S是弱酸,故非金属性:Cl>S
④X元素的阳离子和Y元素的阴离子具有相同的电子层结构,则原子序数:X>Y
⑤O2和O3属于同素异形体,故它们的性质相同.
| A. | ①④ | B. | ①③⑤ | C. | ①②④ | D. | ②④ |
19.下列对Na2CO3和NaHCO3溶液说法中不正确的是( )
| A. | 在Na2CO3和NaHCO3溶液中离子种类相同 | |
| B. | 在溶质物质的量浓度和体积相等的Na2A和NaHA溶液中,阴离子总数相等 | |
| C. | 在NaHCO3溶液中一定有:c(Na+)+c(H+)═c(HCO3-)+c(OH-)+2 c(CO32-) | |
| D. | 在Na2CO3溶液中一定有:c(OH-)═c(H+)+c(HCO3-)+2c(H2CO3) |
13.设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个N2分子和NA个CO2原子个数比为1:1 | |
| B. | 1 mol H2O的质量与NA个H2O质量的总和几乎相等 | |
| C. | 1mol H2所含的原子数为NA | |
| D. | 1mol H2SO4中所含的粒子数目一定是NA |
 图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: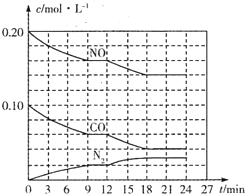 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.