题目内容
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+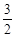 O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
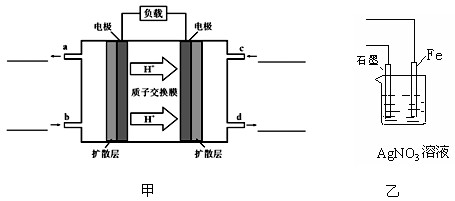
请回答下列问题:
(1)写出甲图中b、c两个入口通入的物质名称(或化学式)b c
(2)负极的电极反应式为
(3)用该原电池电解AgNO3溶液,若Fe电极增重5.4g,则燃料电池在理论上消耗的氧气的体积为 mL(标准状况)
 O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
请回答下列问题:
(1)写出甲图中b、c两个入口通入的物质名称(或化学式)b c
(2)负极的电极反应式为
(3)用该原电池电解AgNO3溶液,若Fe电极增重5.4g,则燃料电池在理论上消耗的氧气的体积为 mL(标准状况)
①b 甲醇水溶液 c 氧气(2分)
②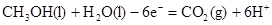 (2分)③ 280 mL(2分)
(2分)③ 280 mL(2分)
②
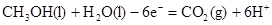 (2分)③ 280 mL(2分)
(2分)③ 280 mL(2分)(1)由于原电池中氢离子向右侧移动,所以右侧是正极,左侧是负极。因此则b通入甲醇,因此c通入氧气。
(2)负极失去电子,所以方程式为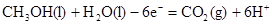 。
。
(3)Fe电极增重5.4g,说明析出银是5.4g,则转移电子是5.4g÷108g/mol=0.05mol,所以根据电子得失守恒可知,消耗氧气是0.05mol÷4=0.0125mol,体积是0.0125mol×22.4L/mol=0.28L=280ml。
(2)负极失去电子,所以方程式为
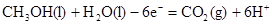 。
。(3)Fe电极增重5.4g,说明析出银是5.4g,则转移电子是5.4g÷108g/mol=0.05mol,所以根据电子得失守恒可知,消耗氧气是0.05mol÷4=0.0125mol,体积是0.0125mol×22.4L/mol=0.28L=280ml。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
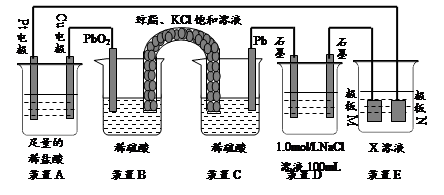
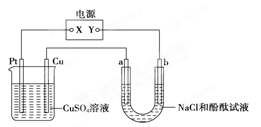
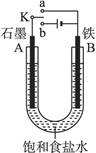
 下图为化学能与电能相互转化的装置示意图。
下图为化学能与电能相互转化的装置示意图。