题目内容
(14分)  下图为化学能与电能相互转化的装置示意图。
下图为化学能与电能相互转化的装置示意图。

 (1)在甲图中,锌极为________极(填“正”或
(1)在甲图中,锌极为________极(填“正”或 “负”),该极的电极反应式是_____________________;随着反应的进行,溶液的pH值________(填“变大”或“变小” 或“不变”)。
“负”),该极的电极反应式是_____________________;随着反应的进行,溶液的pH值________(填“变大”或“变小” 或“不变”)。
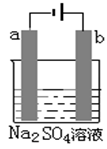
 (2)在乙图中,a和b均为石墨电极。接通电源一段时间后,发现a极有无色无味的气体生成。则电源的M极为______极,b电极的电极反应式是________________,乙装置中发生的总反应的化学方程式为 。假如电路中有4 mol电子通过,a电极理论上析出气体的体积是__________L(标准状况)。
(2)在乙图中,a和b均为石墨电极。接通电源一段时间后,发现a极有无色无味的气体生成。则电源的M极为______极,b电极的电极反应式是________________,乙装置中发生的总反应的化学方程式为 。假如电路中有4 mol电子通过,a电极理论上析出气体的体积是__________L(标准状况)。
 下图为化学能与电能相互转化的装置示意图。
下图为化学能与电能相互转化的装置示意图。
 (1)在甲图中,锌极为________极(填“正”或
(1)在甲图中,锌极为________极(填“正”或 “负”),该极的电极反应式是_____________________;随着反应的进行,溶液的pH值________(填“变大”或“变小” 或“不变”)。
“负”),该极的电极反应式是_____________________;随着反应的进行,溶液的pH值________(填“变大”或“变小” 或“不变”)。 (2)在乙图中,a和b均为石墨电极。接通电源一段时间后,发现a极有无色无味的气体生成。则电源的M极为______极,b电极的电极反应式是________________,乙装置中发生的总反应的化学方程式为 。假如电路中有4 mol电子通过,a电极理论上析出气体的体积是__________L(标准状况)。
(2)在乙图中,a和b均为石墨电极。接通电源一段时间后,发现a极有无色无味的气体生成。则电源的M极为______极,b电极的电极反应式是________________,乙装置中发生的总反应的化学方程式为 。假如电路中有4 mol电子通过,a电极理论上析出气体的体积是__________L(标准状况)。(1)负 Zn—2e—=Zn2+ 变大
(2) 负 2Cl——2e—=Cl2↑ 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 44.8L
2NaOH+H2↑+Cl2↑ 44.8L
(2) 负 2Cl——2e—=Cl2↑ 2NaCl+2H2O
 2NaOH+H2↑+Cl2↑ 44.8L
2NaOH+H2↑+Cl2↑ 44.8L(1)在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以锌是负极,失去电子,被氧化。石墨是正极,溶液中的氢离子在正极得到电子,生成氢气,所以溶液的酸性会降低,pH变大。
(2)a极有无色无味的气体生成,说明a极是阴极,氢离子放电生成氢气,因此M是电源的负极,N是正极,b是阳极,溶液中的氯离子放电,生成氯气。根据电极反应式可知,当电路中有4 mol电子通过时,生成氢气和氯气都是2mol,所以其体积在标准状况下都是2mol×22.4L/mol=44.8L。
(2)a极有无色无味的气体生成,说明a极是阴极,氢离子放电生成氢气,因此M是电源的负极,N是正极,b是阳极,溶液中的氯离子放电,生成氯气。根据电极反应式可知,当电路中有4 mol电子通过时,生成氢气和氯气都是2mol,所以其体积在标准状况下都是2mol×22.4L/mol=44.8L。

练习册系列答案
相关题目
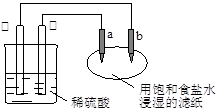
 O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下: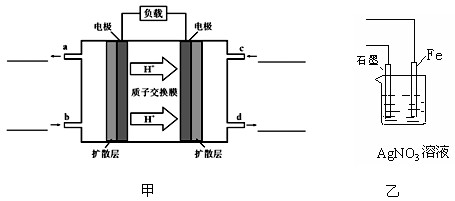
 Fe(OH)2 +Ni(OH)2 下列推断中正确的是
Fe(OH)2 +Ni(OH)2 下列推断中正确的是 Cd(OH)2(s) + 2 Ni(OH)2(s)
Cd(OH)2(s) + 2 Ni(OH)2(s)