题目内容
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )
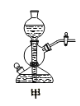
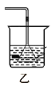
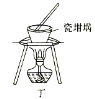
A. 用甲装置实验室制取乙炔 B. 盛有水的乙装置,吸收HCl气体
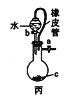
C. 用丙装置测量气体可以减少误差 D. 用丁装置蒸发MgCl2溶液
【答案】C
【解析】
A项,实验室用碳化钙与水反应制取乙炔,此反应剧烈,大量放热,会损坏启普发生器,生成的氢氧化钙是糊状物,会堵塞反应容器,所以不能利用启普发生器制取乙炔,故A不能达到实验目的;
B项,用如图盛有水的装置吸收HCl气体,会引起倒吸,故B不能达到实验目的;
C项,丙装置中,分液漏斗和烧瓶之间用橡皮管连接,可以防止因向烧瓶中加入液体而引起气体体积的变化,故用丙装置测量气体可以减少误差,故C能达到实验目的;
D项,蒸发操作一般要用蒸发皿,加热蒸发MgCl2溶液时,加热促进水解:MgCl2+2H2O![]() Mg(OH)2+2HCl,由于HCl不断挥发,所以得不到MgCl2,故D不能达到实验目的。
Mg(OH)2+2HCl,由于HCl不断挥发,所以得不到MgCl2,故D不能达到实验目的。
综上所述,符合题意的选项为C。

练习册系列答案
相关题目
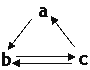
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 选项 | a | b | c |
A | Al | AlCl3 | Al(OH)3 | |
B | CO2 | Na2CO3 | NaHCO3 | |
C | Si | SiO2 | H2SiO3 | |
D | S | SO3 | H2SO4 |
A. A B. B C. C D. D