题目内容
11.利用如图装置收集下列各种气体并进行相应性质实验,你认为发生的现象和得出的结论合理的是( )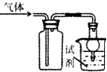
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | X | 澄清石灰水 | 溶液变浑浊 | X一定是CO2 |
| B | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2具有酸性和漂白性 |
| C | NO2 | KI淀粉溶液 | 溶液变为蓝色 | NO2水溶液具有氧化性 |
| D | NH3 | 酚酞试液 | 溶液变为红色 | NH3属于碱 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化碳、二氧化硫都可与氢氧化钙反应生成沉淀;
B.干燥的氯气不具有漂白性;
C.二氧化氮和水反应生成具有氧化性的硝酸;
D.氨气密度比空气小,应用向下排空法收集.
解答 解:A.能使澄清石灰水变浑浊的气体不一定为CO2,也可能为SO2,故A错误;
B.氯气与水反应生成盐酸和次氯酸,但干燥的氯气不具有漂白性,故B错误;
C.二氧化氮和水反应生成硝酸,具有强氧化性,可氧化KI,故C正确;
D.氨气密度比空气小,应用向下排空法收集,故D错误.
故选C.
点评 本题综合考查物质的性质检验,为高考常见题型,侧重于学生的分析能力、实验能力的考查,注意把握物质的性质以及实验的严密性、可行性的评价,难度中等.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
1.在一含Na+的澄清溶液中,可能还存在NH4+、Fe2+、I-、Br-、CO32-、SO32-六种离子中的几种.
①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;
②向上述呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;
③橙黄色溶液不能使淀粉溶液变蓝色.
根据上述实验事实推断,下列说法不正确的是( )
①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;
②向上述呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;
③橙黄色溶液不能使淀粉溶液变蓝色.
根据上述实验事实推断,下列说法不正确的是( )
| A. | 溶液中一定存在Br-、CO32- | B. | 溶液中一定存在NH4+ | ||
| C. | 溶液中一定不存在Fe2+、I-、SO32- | D. | 溶液中可能存在NH4+ |
19.现代化学键理论认为苯环结构中不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
6.已知下述三个实验中的物质均能发生化学反应.
下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 实验③中反应的离子方程式为Fe+Fe3+═2Fe2+ | |
| C. | 实验②中Fe2+既显氧化性又显还原性 | |
| D. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
16.已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下:下列说法不正确的( )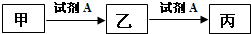
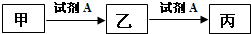
| A. | 若A为硝酸,X为金属元素,则甲与丙反应可生成乙 | |
| B. | 若乙为NaHCO3,则丙一定是CO2 | |
| C. | 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质 | |
| D. | 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
3.从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法有( )
| A. | 加入适量的FeCl2溶液 | B. | 加入适量的KBr溶液 | ||
| C. | 加入适量的饱和食盐水 | D. | 加入适量的Na2S溶液 |
20.下列与物质分类相关的说法正确的是( )
| A. | 只含一种分子的物质一定是纯净物 | |
| B. | 由Na2O2制取O2一定要加入氧化剂 | |
| C. | 金属氧化物一定是碱性氧化物 | |
| D. | 含氧酸受热分解都能生成对应的酸酐和水 |
