题目内容
【题目】工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。

(1)写出仪器的名称:a_______________,b___________________。
(2)A中反应的化学方程式为____________。
(3)装置B中加入的试剂是_____________。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置______和 ________(填字母)间增加一个盛有________的洗气瓶。
(5)装置D的作用是___________________。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:___________。
【答案】分液漏斗 圆底烧瓶 MnO2+4HCl(浓)![]() MnCl2+2H2O+ Cl2 ↑ 浓硫酸 A B 饱和食盐水 吸收未反应的氯气(或对氯气进行尾气处理) 将D装置改为盛有碱石灰的球形干燥管(或在C和D之间增加一个盛有浓硫酸的洗气瓶)
MnCl2+2H2O+ Cl2 ↑ 浓硫酸 A B 饱和食盐水 吸收未反应的氯气(或对氯气进行尾气处理) 将D装置改为盛有碱石灰的球形干燥管(或在C和D之间增加一个盛有浓硫酸的洗气瓶)
【解析】
装置A是制备氯气的发生装置,生成的氯气中含氯化氢和水蒸气,通过装置B中浓硫酸干燥氯气,通过装置C中氯气和铁屑反应生成无水氯化铁,玻璃丝可以收集升华的无水氯化铁,但此时HCl气体没有除去,会影响无水氯化铁的纯度,所以需要在A和B之间加一个除去HCl的装置,然后再和铁反应;剩余气体通过氢氧化钠溶液吸收。
(1)由仪器的构造可知a为分液漏斗,b为圆底烧瓶;
(2)A装置制取的是氯气,实验室常用浓盐酸与二氧化锰加热制取,化学反应方程式为:MnO2+4HCl(浓)![]() MnCl2+2H2O+ Cl2 ↑;
MnCl2+2H2O+ Cl2 ↑;
(3)为制备无水氯化铁,B装置应为盛有浓硫酸的干燥氯气的装置;
(4)制备的氯气中混有氯化氢气体,所以需在干燥之前除氯化氢,故在A与B间添加盛有饱和食盐水的洗气瓶;
(5)氯气污染空气,D装置用氢氧化钠除未反应完的氯气;为制备无水氯化铁,防止水蒸气进入C装置,可将D装置改为盛有碱石灰的球形干燥管,既能吸收氯气,又能吸水,或在装置C和D之间增加一个盛有浓硫酸的洗气瓶。

【题目】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
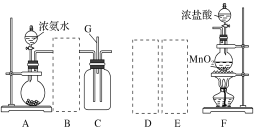
请回答下列问题:
(1)装置A中的烧瓶内固体可选用________(填字母)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(2)虚线框内应添加必要的除杂装置,请从如图的备选装置中选择,并将编号填入下列空格:
备选装置 | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
B:________、D:________、E:________。
(3)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:_______
(4)装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案确定该白色固体中的阳离子:________________