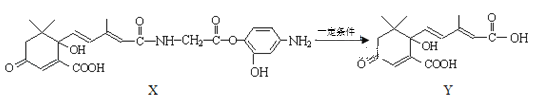
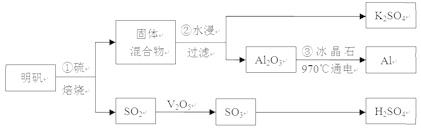
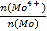题目内容
【题目】常温下向10mL ![]() 的HR溶液中逐滴滴入
的HR溶液中逐滴滴入![]() 的
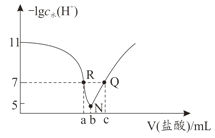
的![]() 溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是
溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是![]()

A.![]() 点导电能力增强说明HR为弱酸
点导电能力增强说明HR为弱酸
B.b点溶液![]() 说明
说明![]() 没有水解
没有水解
C.c 点溶液存在![]() 、
、![]()
D.![]() 任意点溶液均有
任意点溶液均有![]()
![]()
【答案】B
【解析】
A.溶液导电能力与离子浓度成正比,如果HR是强电解质,加入氨水至溶液呈中性时,溶液中离子浓度会减小,导致溶液导电能力降低,根据图知,加入氨水至溶液呈中性时随着氨水的加入,溶液导电能力增强,说明离子浓度增大,则HR为弱电解质,故A正确;
B.弱离子在水溶液中会发生水解反应,根据A知,HR是弱电解质,且一水合氨是弱电解质,所以![]() 是弱酸弱碱盐,b点溶液呈中性,且此时二者的浓度、体积都相等,说明HR和一水合氨的电离程度相等,所以该点溶液中铵根离子和酸根离子水解程度相等,故B错误;
是弱酸弱碱盐,b点溶液呈中性,且此时二者的浓度、体积都相等,说明HR和一水合氨的电离程度相等,所以该点溶液中铵根离子和酸根离子水解程度相等,故B错误;
C.c点溶液的![]() ,说明溶液呈碱性,溶液中
,说明溶液呈碱性,溶液中![]() ,再结合电荷守恒得
,再结合电荷守恒得![]() ,故C正确;
,故C正确;
D.离子积常数只与温度有关,温度不变,离子积常数不变,所以![]() 任意点溶液均有
任意点溶液均有![]()
![]() ,故D正确;
,故D正确;
故选B。

练习册系列答案
相关题目