题目内容
恒温、恒压下,n molA和1molB在一个容积可变的容器中发生如下反应:
A(g)+2B(g)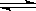 2C(g) 一段时间后达到平衡,生成amolC。则下列说法中正确的是:
2C(g) 一段时间后达到平衡,生成amolC。则下列说法中正确的是:
A.物质A、B的转化率之比为1:2
B.当ν正(A)=2ν逆(C)时,可断定反应达到平衡
C.若起始时放入3nmolA和3molB,则达平衡时生成3amolC
D.起始时刻和达平衡后容器中的压强比为(1+n):(1+n—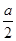 )
)
A(g)+2B(g)
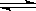 2C(g) 一段时间后达到平衡,生成amolC。则下列说法中正确的是:
2C(g) 一段时间后达到平衡,生成amolC。则下列说法中正确的是:A.物质A、B的转化率之比为1:2
B.当ν正(A)=2ν逆(C)时,可断定反应达到平衡
C.若起始时放入3nmolA和3molB,则达平衡时生成3amolC
D.起始时刻和达平衡后容器中的压强比为(1+n):(1+n—
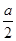 )
)C
生成amolC,则消耗AB的物质的量分别是0.5amol和amol,所以物质A、B的转化率分别是a/2n和a,则A不正确;B中反应速率的方向相反,但不满足反应速率之比时相应的化学计量数之比,B不正确;由于温度和压强不变,且AB的起始量之比相等,所以反应是等效的,C正确;由于是保持恒压,所以压强是不变的,D不正确,答案选C。

练习册系列答案
相关题目
 2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是
2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是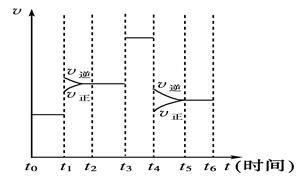
 R(g)+S(s)在恒温下已达到平衡的是( )
R(g)+S(s)在恒温下已达到平衡的是( ) 2XY2
2XY2
 zC(g),达到平衡时,测的A的浓度为0.5mol/L,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测的A的浓度降低为0.3mol/L,下列有关判断正确的是
zC(g),达到平衡时,测的A的浓度为0.5mol/L,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测的A的浓度降低为0.3mol/L,下列有关判断正确的是 2NH3(g)△H=" —92.4" kJ/mol。
2NH3(g)△H=" —92.4" kJ/mol。