题目内容
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4 (s)![]() 2NH3 (g)+ CO2 (g) 。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3 (g)+ CO2 (g) 。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
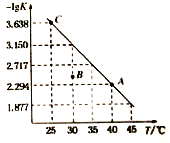
A. C点对应状态的平衡常数K(C)=10-3.638
B. 该反应的△H>0
C. NH3的体积分数不变时,该反应一定达到平衡状态
D. 30 ℃时,B点对应状态的v(正)<v(逆)
【答案】C
【解析】A、C点对应平衡常数的负对数(-lgK)=3.638,所以C点对应状态的平衡常数K(C)=10-3.638,A正确;B、温度升高平衡常数的负对数(-lgK)减小,即温度越高K值越大,所以正反应是吸热反应,则△H>0,B正确;C、体系中两种气体的物质的量之比始终不变,所以NH3的体积分数不变时,该反应不一定达到平衡状态,C错误;D、30℃时,B点未平衡,最终要达平衡状态,平衡常数的负对数要变大,所以此时的(-lgQC)<(-lgK),所以QC>K,因此B点对应状态的v(正)<v(逆),D正确;答案选C。

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目