题目内容
13.氧化钙和盐酸反应方程式为CaO+2HCl=CaCl2+H2O.分析 氧化钙为碱性氧化物与盐酸反应生成氯化钙和水,据此写出反应方程式.
解答 解:氧化钙与盐酸反应生成氯化钙和水,反应方程式:CaO+2HCl=CaCl2+H2O;
故答案为:CaO+2HCl=CaCl2+H2O.
点评 本题考查了化学方程式的书写,明确氧化钙为碱性氧化物,熟悉碱性氧化物的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
4.在容积固定为2L的密闭容器中,充入0.180molHI,480℃时反应:2HI(g)?H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
反应进行至10min后将反应混合物的温度降低,发现气体的颜色变浅.
(1)0~2min内H2的平均反应速度为0.002mol/(L•min).达平衡时,HI的转化率是22.2%.
(2)当上述反应达平衡时,降低温度,原化学平衡向逆向移动(填“正向”,“逆向”或“不”),上述正向反应是:吸热反应(选填:放热、吸热),逆反应速率减小(填“增大”、“减小”或“不变”).
(3)480℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K的值为49.
(4)要增大反应2HI(g)?H2(g)+I2(g)的平衡常数,可采取的措施是D(选填字母).
A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度.
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
(1)0~2min内H2的平均反应速度为0.002mol/(L•min).达平衡时,HI的转化率是22.2%.
(2)当上述反应达平衡时,降低温度,原化学平衡向逆向移动(填“正向”,“逆向”或“不”),上述正向反应是:吸热反应(选填:放热、吸热),逆反应速率减小(填“增大”、“减小”或“不变”).
(3)480℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K的值为49.
(4)要增大反应2HI(g)?H2(g)+I2(g)的平衡常数,可采取的措施是D(选填字母).
A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度.
8.卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法不正确的是( )
| A. | 卤素单质的沸点按F2、Cl2、Br2、I2的顺序依次增大 | |
| B. | 卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难 | |
| C. | 卤化氢的热稳定性和还原性按HF、HCl、HBr、HI的顺序依次减弱 | |
| D. | 卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
18.下列装置或操作正确,且能达到目的是( )
| A. |  依据褪色快慢比较浓度对反应速率的影响 | |
| B. |  测定盐酸浓度 | |
| C. | 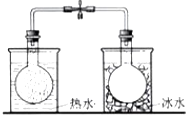 依据气体颜色变化,证明温度对平衡移动的影响 | |
| D. |  中和热的测定 |
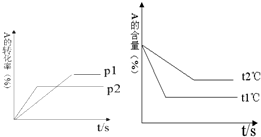 可逆反应:aA(g)+bB(g) cC(g)+dD(g);根据图回答:
可逆反应:aA(g)+bB(g) cC(g)+dD(g);根据图回答:
