题目内容
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究:
途径a:
途径b:
下列有关说法不正确的是( )
途径a:

途径b:

下列有关说法不正确的是( )
| A、1.92g固体只含Cu |
| B、由Ⅰ可知X中一定存在Fe2O3和Cu |
| C、原混合物中m(Fe2O3):m(Cu)=1:1 |
| D、原混合物X至少含Al2O3和SiO2中的一种,但不能进一步确认二者的存在与否 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:途径a:9.4gX和过量盐酸反应生成蓝色溶液,所以是铜离子的颜色,但是金属Cu和盐酸不反应,所以一定含有氧化铁,和盐酸反应生成的三价铁离子可以和金属铜反应,二氧化硅可以和氢氧化钠反应,4.92g固体和氢氧化钠反应后,固体质量减少了3.0g,所以该固体为二氧化硅,质量为3.0g,涉及的反应有:Fe2O3+6H+=2Fe3++3H2O;Cu+2Fe3+=2Fe2++Cu2+,SiO2+2NaOH=Na2SiO3+H2O,又Cu与NaOH不反应,1.92g固体只含Cu;结合途径b可知9.4gX和过量的氢氧化钠反应,固体质量变为6.4g,所以固体只有二氧化硅,一定没有氧化铝;
途径b:9.4gX与过量的氢氧化钠溶液反应后得到6.4g不溶物,固体部分溶解,原固体中至少含有Al2O3、SiO2的一种物质;6.4g固体与过量的盐酸反应得到蓝色溶液,蓝色溶液中存在铜离子,发生了反应:Fe2O3+6H+═2Fe3++3H2O、Cu+2Fe3+═2Fe2++Cu2+,说明溶液中一定存在Fe2O3,则1.92g固体为铜,以此来解答.
途径b:9.4gX与过量的氢氧化钠溶液反应后得到6.4g不溶物,固体部分溶解,原固体中至少含有Al2O3、SiO2的一种物质;6.4g固体与过量的盐酸反应得到蓝色溶液,蓝色溶液中存在铜离子,发生了反应:Fe2O3+6H+═2Fe3++3H2O、Cu+2Fe3+═2Fe2++Cu2+,说明溶液中一定存在Fe2O3,则1.92g固体为铜,以此来解答.
解答:
解:途径a:9.4gX和过量盐酸反应生成蓝色溶液,所以是铜离子的颜色,但是金属Cu和盐酸不反应,所以一定含有氧化铁,和盐酸反应生成的三价铁离子可以和金属铜反应,二氧化硅可以和氢氧化钠反应,4.92g固体和氢氧化钠反应后,固体质量减少了3.0g,所以该固体为二氧化硅,质量为3.0g,涉及的反应有:Fe2O3+6H+=2Fe3++3H2O;Cu+2Fe3+=2Fe2++Cu2+,SiO2+2NaOH=Na2SiO3+H2O,又Cu与NaOH不反应,1.92g固体只含Cu;结合途径b可知9.4gX和过量的氢氧化钠反应,固体质量变为6.4g,所以固体只有二氧化硅,一定没有氧化铝;
途径b:9.4gX与过量的氢氧化钠溶液反应后得到6.4g不溶物,固体部分溶解,原固体中至少含有Al2O3、SiO2的一种物质;6.4g固体与过量的盐酸反应得到蓝色溶液,蓝色溶液中存在铜离子,发生了反应:Fe2O3+6H+═2Fe3++3H2O、Cu+2Fe3+═2Fe2++Cu2+,说明溶液中一定存在Fe2O3,则1.92g固体为铜,
A.由上述分析可知,1.92g固体只含Cu,故A正确;
B.由I可知,X和过量盐酸反应生成蓝色溶液,为铜离子的颜色,但Cu和盐酸不反应,则一定含有氧化铁,和盐酸反应生成的三价铁离子和金属铜反应,即X中一定存在Fe2O3和Cu,故B正确;
C.设氧化铁的物质的量是x,金属铜的物质的量是y,由Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+得出:Fe2O3~2Fe3+~Cu,则160x+64y=6.4,64y-64x=1.92,解得x=0.02mol,y=0.05mol,所以氧化铁的质量为0.02mol×160g/mol=3.2g,金属铜的质量为0.05mol×64g/mol=3.2g,则原混合物中m(Fe2O3):m(Cu)=1:1,故C正确;
D.由上述分析可知,混合物中只有二氧化硅,一定没有氧化铝,故D错误;
故选D.
途径b:9.4gX与过量的氢氧化钠溶液反应后得到6.4g不溶物,固体部分溶解,原固体中至少含有Al2O3、SiO2的一种物质;6.4g固体与过量的盐酸反应得到蓝色溶液,蓝色溶液中存在铜离子,发生了反应:Fe2O3+6H+═2Fe3++3H2O、Cu+2Fe3+═2Fe2++Cu2+,说明溶液中一定存在Fe2O3,则1.92g固体为铜,
A.由上述分析可知,1.92g固体只含Cu,故A正确;
B.由I可知,X和过量盐酸反应生成蓝色溶液,为铜离子的颜色,但Cu和盐酸不反应,则一定含有氧化铁,和盐酸反应生成的三价铁离子和金属铜反应,即X中一定存在Fe2O3和Cu,故B正确;
C.设氧化铁的物质的量是x,金属铜的物质的量是y,由Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+得出:Fe2O3~2Fe3+~Cu,则160x+64y=6.4,64y-64x=1.92,解得x=0.02mol,y=0.05mol,所以氧化铁的质量为0.02mol×160g/mol=3.2g,金属铜的质量为0.05mol×64g/mol=3.2g,则原混合物中m(Fe2O3):m(Cu)=1:1,故C正确;
D.由上述分析可知,混合物中只有二氧化硅,一定没有氧化铝,故D错误;
故选D.
点评:本题考查了物质的成分推断及有关化学反应的简单计算,题目难度中等,注意掌握检验未知物的采用方法,能够根据反应现象判断存在的物质,选项D为难点和易错点,注意合理分析题中数据,根据题中数据及反应方程式计算出铜和氧化铁的质量.

练习册系列答案
相关题目
金属的冶炼常涉及氧化还原反应.由下列物质冶炼相应金属时采用电解法的是( )
| A、Al2O3 |
| B、HgO |
| C、Cu2S |
| D、Fe2O3 |
下列与有机物结构、性质相关的叙述错误的是( )
A、乙醛和丙烯醛(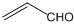 )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B、一分子β-月桂烯(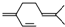 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C、用甘氨酸(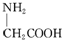 )和丙氨酸( )和丙氨酸(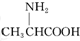 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D、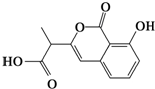 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
下列说法正确的是( )
| A、浓硫酸溶于水的过程属于放热反应 |
| B、既有化学键断裂又有化学键生成的过程一定属于化学反应 |
| C、物质导电的过程一定是物理变化 |
| D、同分异构体之间的相互转化一定是化学变化 |
下列实验现象的描述错误的是( )
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、红热的铁丝在氯气中燃烧,火星四射,生成黑色固体颗粒 |
| C、红热的铜丝在氯气中燃烧,产生棕黄色烟 |
| D、钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是( )
| A、CH3CH2OH |
B、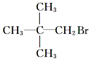 |
C、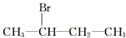 |
D、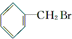 |
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金--氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出.其反应原理为
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
| A、Na[Au(CN)2]不溶于水 |
| B、化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C、金元素在地壳中能以化合态的形式存在 |
| D、在提炼过程中含金元素的物质始终作氧化剂 |
下列叙述正确的是( )
| A、乙烯、聚氯乙烯和苯分子中均含有碳碳双键 |
| B、淀粉、油脂、蛋白质都是天然高分子化合物且都能水解 |
| C、在蛋白质溶液中加入硫酸铜溶液,蛋白质会发生凝聚,加水后不能再溶解 |
| D、用氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸 |
