题目内容
4.将5.6g铁粉投入盛有100mL 2mol•L-1稀硫酸的烧杯中,2min时铁粉刚好溶解完全,如果反应前后溶液的体积不变,则该反应的平均速率可表示为( )| A. | v(Fe)=0.5mol•(L•min)-1 | B. | v(H2SO4)=1mol•(L•min)-1 | ||
| C. | v(H2)=0.5mol•(L•min)-1 | D. | v=(FeSO4)=0.5mol•(L•min)-1 |
分析 Fe为固体,浓度不变,不能利用浓度变化量表示反应速率,不能计算氢气浓度,也不能用氢气表示平均速率,根据方程式计算硫酸、硫酸铁的物质的量变化量,再根据v=$\frac{\frac{△n}{V}}{△t}$计算2min内平均速率.
解答 解:5.6gFe的物质的量为$\frac{5.6g}{56g/mol}$=0.1mol,
Fe+H2SO4=Fe2SO4+H2↑
0.1mol 0.1mol 0.1mol
A.Fe为固体,浓度不变,不能利用浓度变化量表示反应速率,故A错误;
B.硫酸浓度变化量为$\frac{0.1mol}{0.1L}$=1mol/L,故v(H2SO4)=$\frac{1mol/L}{2min}$=0.5 mol•L-1•min-1,故B错误;
C.不能计算氢气浓度,不能用氢气表示平均速率,故C错误;
D.硫酸亚铁的浓度变化量为为$\frac{0.1mol}{0.1L}$=1mol/L,故v(FeSO4)=$\frac{1mol/L}{2min}$=0.5 mol•L-1•min-1,故D正确,
故选D.
点评 本题考查化学反应速率的有关计算,难度不大,注意对速率公式的理解掌握,有利于基础知识的巩固.

练习册系列答案
相关题目
14.下列现象中,不是因为发生化学反应而产生的是( )
| A. | 将苯滴入溴水中,振荡后水层接近无色 | |
| B. | 乙烯使酸性KMnO4溶液褪色 | |
| C. | 乙烯使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
12.标准状况下,由甲烷和乙烯组成的混合气体,其密度为1g•L-1,则该混合气体中甲烷与乙烯的质量比为( )
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |
5.已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )
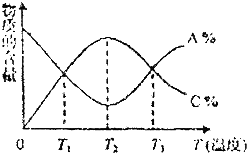

| A. | 该反应在T1、T3温度时达到过化学平衡 | |
| B. | 该反应的正反应是吸热反应 | |
| C. | 该反应在T2温度时达到过化学平衡 | |
| D. | 升高温度,平衡会向正反应方向移动 |
12.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放上蒸发皿;②放置酒精灯;③固定铁圈位置;④加热搅拌;⑤停止加热、余热蒸干.其正确操作的顺序是( )
| A. | ②①③④⑤ | B. | ①②③④⑤ | C. | ②③①④⑤ | D. | ③②①④⑤ |
10.化学反应前后发生变化的是( )
| A. | 原子个数 | B. | 元素种类 | C. | 质量 | D. | 化学键 |