题目内容
【题目】氢在生活、生产、科研中发挥着重要的作用。
Ⅰ.工业上利用吸热反应C(s) +2H2O(g)![]() CO2(g)+2H2(g)来制备氢气。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,相关数据如下表:
CO2(g)+2H2(g)来制备氢气。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,相关数据如下表:
容器 | 容积/L | 温度/L | 起始量/mol | 平衡量/mol | |
C(s) | H2O(g) | H2(g) | |||
甲 | 2 | T1 | 3 | 4 | 3.2 |
乙 | 1 | T2 | 1.5 | 2 | 1.2 |
(l)T1_______T2 (填“>”、“ =”或“<”)。
(2)T1时达到平衡后再加入lmolH2O(g),达到新平衡后H2(g)的物质的量分数__________(填“增大”、“ 不变”或“减小”);T2时,若起始时乙容器中加入1.5molC(s)、1.2molH2O(g)、0.5molCO2(g)、1.4molH2(g),此时v(正)________v(逆)(填“大 于”、“ 等 于” 或“小于”)。
Ⅱ.CO(g)和H2(g)在一定条件下可合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
(3)该反应能量变化曲线如图所示,下列叙述正确的是___________。
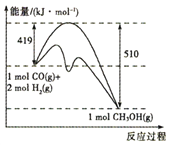
A.该反应的△H>0
B.该反应的活化能为419kJ
C.使用催化剂后反应速率加快,△H 不变
D.若改变条件使平衡向正反应方向移动,则CO 的转化率可能增大,可能不变,也可能减小
(4)反应分別在230℃、250℃、270℃进行时,CO的平衡转化率与![]() 的关系如图所示。
的关系如图所示。
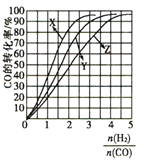
①230℃对应的曲线是_________________,依据是________________。
②向容积为1L的密闭容器中投入1nolCO、3molH2,在上述某温度下进行反应,平衡后测得![]() =
=![]() ,则反应温度为_____________,平衡常数K=_________________。
,则反应温度为_____________,平衡常数K=_________________。
【答案】 > 减小 小于 CD X 对于放热反应,其它条件不变时,温度越低反应物的转化率越高 250℃ 5.625
【解析】(l)根据表中数据甲的体积和起始投料均为乙的二倍,若温度相同则为等效平衡,平衡时氢气的量也应为乙的二倍,则乙中氢气应为1.6mol,实际只有1.2mol,反应为吸热反应,温度降低平衡逆向移动氢气的含量减小,故T1>T2;(2)T1时达到平衡后再加入lmolH2O(g),平衡转移消耗的水比加入的少得多,故达到新平衡后H2(g)的物质的量分数减小;T2时,K=![]() ,若起始时乙容器中加入1.5molC(s)、1.2molH2O(g)、0.5molCO2(g)、1.4molH2(g),此时Q=
,若起始时乙容器中加入1.5molC(s)、1.2molH2O(g)、0.5molCO2(g)、1.4molH2(g),此时Q=![]() ,反应逆向移动,v(正)小于v(逆);(3) A.由图中信息可知,该反应反应物的总能量大于生成物的总能量,故△H<0,选项A错误;B.该反应没有催化剂条件下正反应的的活化能为419kJ/mol,选项B错误;C.使用催化剂后反应速率加快,但催化剂只能改变反应的活化能,不能改变焓变,故△H不变,选项C正确;D.若改变条件使平衡向正反应方向移动,则CO的转化率可能增大,可能不变,也可能减小,选项D正确。答案选CD;(4)①反应CO(g)+2H2(g)
,反应逆向移动,v(正)小于v(逆);(3) A.由图中信息可知,该反应反应物的总能量大于生成物的总能量,故△H<0,选项A错误;B.该反应没有催化剂条件下正反应的的活化能为419kJ/mol,选项B错误;C.使用催化剂后反应速率加快,但催化剂只能改变反应的活化能,不能改变焓变,故△H不变,选项C正确;D.若改变条件使平衡向正反应方向移动,则CO的转化率可能增大,可能不变,也可能减小,选项D正确。答案选CD;(4)①反应CO(g)+2H2(g)![]() CH3OH(g)为放热反应,升高温度反应逆向移动,CO的转化率降低,故230℃对应的曲线是X,依据是对于放热反应,其它条件不变时,温度越低反应物的转化率越高;
CH3OH(g)为放热反应,升高温度反应逆向移动,CO的转化率降低,故230℃对应的曲线是X,依据是对于放热反应,其它条件不变时,温度越低反应物的转化率越高;
②平衡后测得![]() =
=![]() ,设
,设![]() ,
,![]() ,故
,故
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
开始时的浓度(mol/L) 1 3 0
改变的浓度(mol/L) 0.9 3-4x 3x
平衡时的浓度(mol/L) 0.1 4x=1.2 3x=0.9
根据反应有3-4x=2×3x,x=0.3,代入以上数据,则![]() 时,CO的转化率为
时,CO的转化率为![]() ,对应的温度应该为250℃,平衡常数K=
,对应的温度应该为250℃,平衡常数K=![]() 5.625。
5.625。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】如图图象中,纵坐标为沉淀物的物质的悬,横坐标为向溶液中加入反应物的物质的量,则相应的图象序号与(1)﹣(4)对应的是 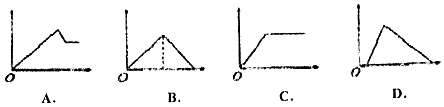
溶液 | 加入物质 | 对应的图象 |
⑴饱和石灰水 | 通过量CO2气体 | |
⑵氯化铝溶液 | 加入过量氨水 | |
⑶MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | |
⑷含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |



