题目内容
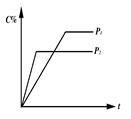
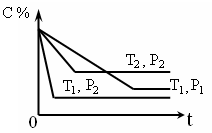
已知某可逆反应:mA(g)+nB(g)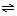 xC(g),在密闭容器中进行,下图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
xC(g),在密闭容器中进行,下图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
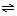 xC(g),在密闭容器中进行,下图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
xC(g),在密闭容器中进行,下图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
| A.T1>T2 ,P1>P2 ,m+n>x,正反应放热 |
| B.T1<T2 ,P1<P2 ,m+n<x,正反应吸热 |
| C.T1>T2 ,P1<P2 ,m+n<x,正反应放热 |
| D.T1<T2 ,P1>P2 ,m+n>x,正反应吸热 |
C
试题分析:根据图像可知,当温度相同时压强为P2的首先达到平衡状态,所以压强PP1<P2但压强高,C的含量低,这说明增大压强,平衡向逆反应方向移动,所以正方应是体积增大的可逆反应,即m+n<x。当压强相同时,温度为T1的首先达到平衡状态,这说明温度是T1>T2 。但温度高,C的含量低,这说明升高温度,平衡向逆反应方向移动,所以正方应是放热反应,答案选C。
点评:在分析有关图像时应该注意:一、ν-t 图像或 c-t 图像:1.ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。 二、平衡图像 1.出现拐点的图像:分析依据“先拐先平”。在转化率-时间图像或物质的百分含量-时间图像中,先出现拐点的曲线先达到平衡(代表温度高或压强大或使用合适的催化剂等)。

练习册系列答案
相关题目

 3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是
3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是 zC达到平衡:
zC达到平衡: 2HI(g)达到化学平衡状态的标志是( )
2HI(g)达到化学平衡状态的标志是( ) 2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是
2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是
 2Z(g)在不同温度和压强下的产物Z的物质的量和反应时
2Z(g)在不同温度和压强下的产物Z的物质的量和反应时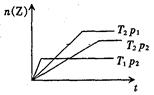
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表: nC(g),C的含量随时间变化情况符合右图所示,下列结论正确的是:
nC(g),C的含量随时间变化情况符合右图所示,下列结论正确的是: