题目内容
某学生设计如下实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
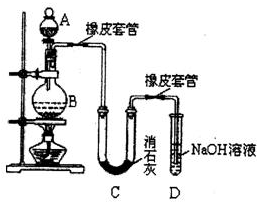
(1)A仪器的名称是
(2)漂白粉将在U型管中产生,其化学反应方程式是
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是
(4)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现主要原因是在U型管中存在两个副反应:温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是

(1)A仪器的名称是
分液漏斗
分液漏斗
,所盛试剂是浓盐酸
浓盐酸
.(2)漂白粉将在U型管中产生,其化学反应方程式是
2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O
2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O
.(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是
氯气易腐蚀橡皮套
氯气易腐蚀橡皮套
.(4)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现主要原因是在U型管中存在两个副反应:温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
将U型管置于冷水浴中
将U型管置于冷水浴中
.分析:(1)A仪器是分液漏斗,所盛试剂为液态反应物;
(2)氯气和氢氧化钙反应生成氯化钙、次氯酸钙、水;
(3)氯气有强氧化性,能腐蚀橡胶;
(4)因为温度高时易生成Ca(ClO3)2,所以避免此反应发生可以采取降温措施.
(2)氯气和氢氧化钙反应生成氯化钙、次氯酸钙、水;
(3)氯气有强氧化性,能腐蚀橡胶;
(4)因为温度高时易生成Ca(ClO3)2,所以避免此反应发生可以采取降温措施.
解答:解:解:(1)A仪器名称是分液漏斗,装置中用分液漏斗添加浓盐酸,所以A是所盛试剂是浓盐酸,
故答案为:分液漏斗;浓盐酸;
(2)漂白粉将在U形管中产生,氯气和氢氧化钙反应生成氯化钙、次氯酸钙、水,其化学方程式为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;
故答案为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;
(3)氯气能和橡胶反应,所以在两个橡皮套管内的玻璃管口应尽量紧靠,故答案为:氯气易腐蚀橡皮套;
(4)温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,用冰水或冷水冷却,故答案为:将U型管置于冷水浴中.
故答案为:分液漏斗;浓盐酸;
(2)漂白粉将在U形管中产生,氯气和氢氧化钙反应生成氯化钙、次氯酸钙、水,其化学方程式为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;
故答案为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;
(3)氯气能和橡胶反应,所以在两个橡皮套管内的玻璃管口应尽量紧靠,故答案为:氯气易腐蚀橡皮套;
(4)温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,用冰水或冷水冷却,故答案为:将U型管置于冷水浴中.
点评:本题考查了实验室制漂白粉的装置分析和制备条件判断,注意信息中温度不同产物不同,难度中等.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
 某学生设计了如图所示的装置进行实验,各装置中所装试剂、实验操作及实验现象如下:
某学生设计了如图所示的装置进行实验,各装置中所装试剂、实验操作及实验现象如下: