题目内容
6.下列有机物中,沸点最高的是( )| A. | 乙醇 | B. | 乙烯 | C. | 乙烷 | D. | 丙烷 |
分析 根据常温下物质的状态进行判断,常温下物质沸点:固体>液态>气态.
解答 解:常温下,乙烯、乙烷、丙烷为气体,而乙醇为液态,故乙醇的沸点最高,故选A.
点评 本题考查物质熔沸点高低比较,比较基础,注意掌握物质熔沸点比较规律.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
16.下列有关化学用语的表示正确的是( )
| A. | 质子数为17,中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 硫离子的结构示意图: | |
| C. | 甲烷分子的比例模型: | |
| D. | 氯乙烯分子的结构简式:CH2-CH2Cl |
17.几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要 化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A. | X、Z、R的最高价氧化物的水化物之间可两两相互反应 | |
| B. | 元素X和Q形成的化合物中不可能含有共价键 | |
| C. | X、Z、M的单质分别与水反应,M最剧烈 | |
| D. | Y的氢化物的水溶液可用于雕刻玻璃 |
14.下列离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
1.下列有关晶体的说法正确的是( )
| A. | 分子晶体中分子间一定存在范德华力 | |
| B. | 晶格能越大,离子晶体的能量越高 | |
| C. | 离子键、共价键、金属键、氢键都是化学键 | |
| D. | 原子间通过共价键形成的晶体一定具有高熔点和高硬度. |
11.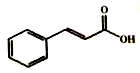 我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
 我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )| A. | 肉桂酸可使酸性高锰酸钾溶液褪色 | |
| B. | 肉桂酸能与银氨溶液发生银镜反应 | |
| C. | 肉桂酸分子式为C7H8O2 | |
| D. | 肉桂酸分子中至少有12个原子共平面 |
18.下列金属冶炼的方法错误的是( )
| A. | 加热分解Ag2O冶炼银 | B. | 用CO还原氧化铁冶炼铁 | ||
| C. | 钠与Mg2Cl溶液反应冶炼镁 | D. | 电解熔融氧化铝冶炼铝 |
4.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0 L 1.0 mol•L-1的NaClO水溶液中含有的氧原子数为NA | |
| B. | 总质量为a g的CO和N2的混合物中所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| C. | 2.24 L的2H35Cl分子中的中子数是1.9NA | |
| D. | 某密闭容器中盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,形成N-H键的数目为0.6NA |