题目内容
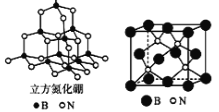
【题目】新型锂空气电池能量密度高、成本低,可作为未来电动汽车的动力源,其工作原理如右图所示。下列有关该电池的说法正确的是

A. 充电时,金属锂为阳极
B. 放电时,正负两极周围都有LiOH
C. 放电时,每消耗22.4LO2,转移4mol电子
D. 放电和充电时,Li+迁移方向相反
【答案】D
【解析】
由图可知,放电时是原电池原理,原电池放电反应为自发的氧化还原反应,即4Li+O2+2H2O=4LiOH,锂为负极,失去电子发生氧化反应Li-e-=Li+,正极上发生得电子的还原反应O2+4e-+2H2O=4OH-;充电时的原理是电解池原理,金属锂电极为阴极,发生还原反应Li+ +e-= Li,阳极反应为4OH--4e-=O2↑+2H2O,以此分析解答。
A. 根据以上分析,充电时,金属锂为阴极,故A错误;
B. 金属锂电极周围为有机电解液,非水溶液,放电时,该极周围不会有LiOH,故B错误;
C. 没有标明是在标准状况下,无法计算22.4LO2的物质的量,故C错误;
D. 放电时阳离子由负极向正极移动,充电时阳离子由阳极向阴极移动,所以Li+迁移方向相反,故D正确。
答案选D。

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。
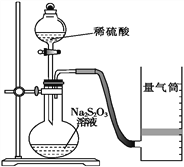
(1)除如图装置所示的实验用品外,还需要的一件实验用品是______________。
(2)圆底烧瓶中所发生反应的离子方程式为___________。
(3)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是____________________________________。
(4)利用该化学反应,试简述测定反应速率的其他方法:________________(写一种)。
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。(已知 I2+2 Na2S2O3=== Na2S4O6+2 NaI,其中Na2S2O3溶液均足量)
实验序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | T1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | T2 |
③ | 6.0 | 2.0 | 4.0 | Vx | T3 |
(5)表中Vx=__________mL,T1、T2、T3的大小关系是____________________________。
【题目】在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ,其化学平衡常数K和温度t的关系如下表:
CO2(g)+H2(g) ,其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 850 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为__________反应(填“吸热”或“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是______________(多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(3)850℃ 时,若向一容积可变的密闭容器中同时充入1.0molCO、3.0molH2O、1.0molCO2
和xmolH2,则:
当x=5.0时,上述平衡向____________(填“正反应”、“逆反应”、“恰好平衡”)方向进行.
② 若要使上述反应开始时向正反应方向进行,则x应满足的条件是_________________.
(4)在850℃时,若设x=5.0mol和x=6.0mol,其他物质的投料不变,当上述反应达到平衡后,
测得H2的体积分数分别为a%、b% ,则a _________ b (填“>”、“<”或“=”)。