题目内容
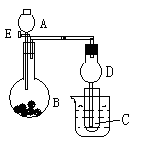
在如右图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有适量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:

(1)实验过程中,观察到的主要现象是:(4分,每空1分)
①____________________________________________________________________________;
②____________________________________________________________________________;
③____________________________________________________________________________;
④____________________________________________________________________________。
(2)欲使反应现象更明显,应向小烧杯中加入___________________。(1分)
A.粗铜片 b.纯铜片
如果反应中加入的是含少量铝的粗铜,则反应中形成无数微电池。请写出微电池中正极上的电极反应方程式_____________________________________________。(3分)
(3)用该装置做铜与浓硝酸反应的实验,最突出的优点是:_______________________。(2分)
(4)若要验证最终得到的气体生成物,最简便的方法是:__________________。(2分)
(5)工业上吸收NO和NO2的混合气体,常使用NaOH溶液。欲使NO和NO2被充分吸收,则NO和NO2的体积应满足_________________。(NO+NO2+2NaOH====2NaNO2+H2O)(3分)
A.V(NO)>V(NO2) b.V(NO)<V(NO2) c.V(NO)≤V(NO2)
答案:(1)①铜片表面产生气泡,铜片慢慢溶解并逐渐消失;②小烧杯中溶液的颜色逐渐变成蓝色;③大烧杯中有红棕色气体生成,后来慢慢变成无色;④大烧杯内液面上升,水槽中液面下降 (4分,每空1分)
(2)a (1分) H++NO3+e-====NO2↑+H2O(3分)
(3)该装置最主要的优点是:反应体系封闭,无氮氧化合物逸出,不污染环境 (2分) (4)轻轻掀起倒扣的大烧杯,放入适量的空气,若有红棕色气体生成,则证明最终气体生成物为NO气体 (2分) (5)c (3分)

 阅读快车系列答案
阅读快车系列答案
 某化学兴趣小组使用酸碱中和滴定法测定市售白醋(主要成分为CH3COOH)的总酸量(g/100ml).
某化学兴趣小组使用酸碱中和滴定法测定市售白醋(主要成分为CH3COOH)的总酸量(g/100ml).
 l溶液各100mL;
l溶液各100mL; )分别稀释至100mL,
)分别稀释至100mL, ·L-1H2SO4 D.2mol·L-1HA
·L-1H2SO4 D.2mol·L-1HA
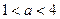 ,则A、B都是弱酸
,则A、B都是弱酸