题目内容
【题目】C是一种合成树脂,高分子化合物,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

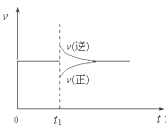
(1)写出A的电子式:____________;D的结构简式为____________。
(2)写出碳化钙与水反应制取A的化学方程式: _______________________。
(3)写出由B生成C的化学方程式: __________________,其反应类型为_________。
【答案】![]() CH2=CH2 CaC2+2H2O→Ca(OH)2+HC≡CH↑ nCH2==CHCl →
CH2=CH2 CaC2+2H2O→Ca(OH)2+HC≡CH↑ nCH2==CHCl →![]() 加聚反应
加聚反应
【解析】
碳化钙与水反应生成乙炔,则气体A为乙炔;D是一种植物生长调节剂,用它可以催熟果实,则D为乙烯;乙炔与HCl加成生成氯乙烯;苯与液溴反应生成溴苯,则E为溴苯;氯乙烯发生加聚反应生成聚氯乙烯,则C为聚氯乙烯。
(1)分析可知,A为乙炔,其电子式为![]() ;D为乙烯,结构简式为CH2=CH2;
;D为乙烯,结构简式为CH2=CH2;
(2) 碳化钙与水生成氢氧化钙和乙炔,方程式为CaC2+2H2O→Ca(OH)2+HC≡CH↑;
(3)氯乙烯在催化剂的条件下发生加聚反应生成聚氯乙烯,方程式为nCH2==CHCl →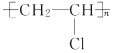 。
。

【题目】已知SO2可以用Fe(NO3)3溶液吸收,按如图所示装置展开相关探究:取一定量的铜片于三颈烧瓶中,通入一段时间N2后再加入足量的浓硫酸,加热;装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀。回答下列问题:
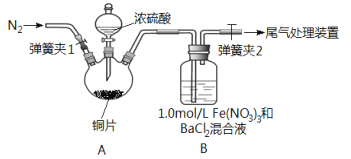
(i)装置A中用于添加浓硫酸的仪器名称为_________________。
(2)实验开始前需进行的操作是_____________________。
(3)加入浓硫酸之前先通入N2一段时间,其目的是_____________________。
(4)排除装置A中白雾影响,可在装置A、B间增加洗气瓶C,则C中盛放的试剂是_______;若用NaOH溶液处理尾气,则发生反应的离子方程式为_________________。
(5)经过讨论,该小组对装置B中产生沉淀的原因,提出下列假设(不考虑各因素的叠加);假设1:装置A中白雾进入装置B中参与了反应;
假设2:______________;
假设3: Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化SO2。
(6)请你设计实验验证上述假设3,写出实验步骤、预期现象和结论。
实验步骤(简述操作过程) | 预期现象和结论 |
①测1.0mol/LFe(NO3)3溶液的pH ②取与Fe(NO3)3溶液中c(NO3-)相同的适量Ba(NO3)2溶液滴入试管中 (3)________________ ④向试管中通入适量SO2气体 | _____________ |
(7)若假设2正确,请写出B中发生反应的离子方程式:_________________。