题目内容
继广州“5.10”化学品仓库爆炸之后,2006年6月15日,一辆满载14t危险化学品的车辆在行驶过程中发生自燃,这两起事故均因化学品“保险粉”而起。“保险粉”又称连二亚硫酸钠,广泛用于纺织工业作还原剂。该化学品在潮湿空气中极不稳定,易分解并引起燃烧,在190℃时发生爆炸反应:2Na2S2O4=Na2S2O3+Na2SO3+SO2↑。工业生产“保险粉”主要用甲酸法,其最主要的步骤是把甲酸(HCOOH)与溶于甲醇(CH3OH)和水混合溶剂中的NaOH混合,再通入SO2气体,所发生的化学反应是:HCOONa+2SO2+NaOH=Na2S2O4+H2O+CO2。下列有关“保险粉”的叙述中错误的是()。
- A.“保险粉”爆炸时发生氧化还原反应
- B.“保险粉”应在通风、干燥、阴凉处密闭贮存
- C.“保险粉”分解时放出二氧化硫,对环境有一定的危害
- D.“保险粉”的还原性比甲酸钠(HCOONa)的还原性强
D

练习册系列答案
相关题目
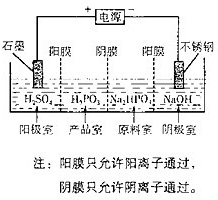 (2013?广州一模)亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3.
(2013?广州一模)亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3.