题目内容
⑴反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1;
FeO(s)+CO(g) △H1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
①反应CO2(g) + H2(g) CO(g) + H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g)
CO(g) + H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
②能判断CO2(g) + H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
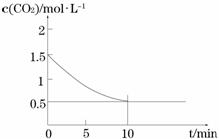 ⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。
① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为_________mol·L-1。
②下列措施中能使平衡时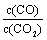 增大的是______(填序号)。
增大的是______(填序号)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
⑴① △H1-△H2 ;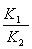 ;吸热 ②B、C ⑵① 2.0 ;0.67(或2/3) ② A
;吸热 ②B、C ⑵① 2.0 ;0.67(或2/3) ② A
(2,2,2,2,2,2,2)

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案右图所示的电解池I和II中,a、b、c和d均为石墨电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b﹤d。符合上述实验结果的盐溶液是( )
| 选项 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |

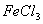 溶液与
溶液与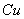 的反应:
的反应: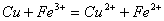
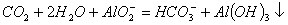
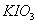 氧化酸性溶液中的
氧化酸性溶液中的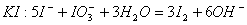
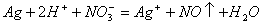
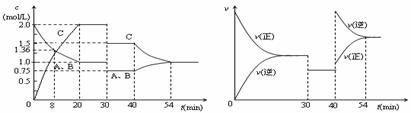

 溶液变为血红色,由此推知A的化学式为__________。
溶液变为血红色,由此推知A的化学式为__________。 _______________________。
_______________________。 E__________、F__________。
E__________、F__________。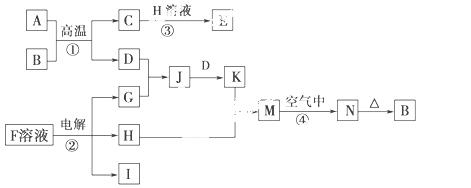
 量酚酞的F的饱和溶液,则在________(填“阴”或“阳”)极附近溶液由无色变为红色,若在此极收集到0.2 g气体,则此时溶液的pH是________(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
量酚酞的F的饱和溶液,则在________(填“阴”或“阳”)极附近溶液由无色变为红色,若在此极收集到0.2 g气体,则此时溶液的pH是________(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。 H
H
 用△H1、△H2和△H3表示
用△H1、△H2和△H3表示