题目内容
人民网2012年11月8日西宁电,青海盐湖海纳化工有限公司15万吨电石项目投产。以电石(CaC2 )为原料可生产许多重要的有机物质,电石可由CaO制得(同时还得到一种可燃性气体物质),有关转化关系如下图所示
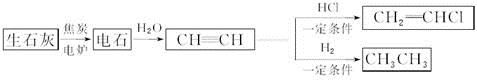
(1)写出制备电石及由电石生成乙炔的化学方程式为__________________、__________________。
(2)基态Ca2+的电子排布式为______________,上面转化关系图中涉及到的元素中,电负性最大的元素是______________,第一电离能最小的元素是________________。
(3)乙炔、乙烷分子中的碳原子杂化类型分别为________________、______________,甲烷的空间构型是________________,该空间构型中,键角__________(填>、<、=)109°28′。
(4)与CH2=CH2相比,CH2=CHCl属于易液化的气体,原因是___________________。
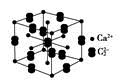
(5)假设下图是电石的晶胞,则一个晶胞中含有________个钙离子,研究表明,亚玲形C的存在,使晶胞沿一个方向拉长,则该晶胞中一个Ca2+周围距离相等且最近的C有________个。

(1)写出制备电石及由电石生成乙炔的化学方程式为__________________、__________________。
(2)基态Ca2+的电子排布式为______________,上面转化关系图中涉及到的元素中,电负性最大的元素是______________,第一电离能最小的元素是________________。
(3)乙炔、乙烷分子中的碳原子杂化类型分别为________________、______________,甲烷的空间构型是________________,该空间构型中,键角__________(填>、<、=)109°28′。
(4)与CH2=CH2相比,CH2=CHCl属于易液化的气体,原因是___________________。
(5)假设下图是电石的晶胞,则一个晶胞中含有________个钙离子,研究表明,亚玲形C的存在,使晶胞沿一个方向拉长,则该晶胞中一个Ca2+周围距离相等且最近的C有________个。

(1)CaO+3C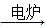 CaC2+CO ↑;CaC2+2H2O—→CH≡CH↑+Ca(OH)2
CaC2+CO ↑;CaC2+2H2O—→CH≡CH↑+Ca(OH)2
(2)1s22s22p63s23p6 O Ca
(3)sp sp3 四面体 =
(4)乙烯与CH2=CHCl均属于分子晶体且组成结构相似,但后者相对分子质量大,范德华力大
(5)4 4
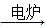 CaC2+CO ↑;CaC2+2H2O—→CH≡CH↑+Ca(OH)2
CaC2+CO ↑;CaC2+2H2O—→CH≡CH↑+Ca(OH)2(2)1s22s22p63s23p6 O Ca
(3)sp sp3 四面体 =
(4)乙烯与CH2=CHCl均属于分子晶体且组成结构相似,但后者相对分子质量大,范德华力大
(5)4 4
(1)CaO与焦炭在电炉中生成CaC2,同时有可燃性CO气体生成;CaC2与H2O反应可以生成乙炔气体。(2)Ca是20号元素,Ca2+有18个电子,基态Ca2+的电子排布式为1s22s22p63s23p6。根据元素的电负性规律可知,非金属元素电负性大于金属元素,非金属性越强,电负性越大,所以电负性最大的元素是O元素;根据元素第一电离能的递变规律可知,金属性越强,电离能越小,所以第一电离能最小的元素为Ca元素。(3)C2H2是直线形分子,C原子杂化方式为sp,C2H6中C原子杂化方式为sp3,甲基是甲烷失去一个氢原子的产物,所以甲烷的空间构型是四面体,键角为109°28′。(4)乙烯与CH2=CHCl组成和结构相似,但CH2=CHCl相对分子质量大,所以范德华力大。(5)该晶胞中顶点占1/8,棱上占1/4,面心占1/2,体心占1,Ca2+为8×1/8+6×1/2=4。根据图像,晶胞沿一个方向拉长,则该晶胞中一个Ca2+周围距离相等且最近的C22-只有同一平面内的4个。

练习册系列答案
相关题目





