题目内容
(10分)已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=_________(填数字表达式)。
下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是____(填字母)。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V盐酸______V醋酸 ,(填“>”、“<”或“=”下同),反应的最初速率为:υ盐酸_______υ醋酸。
(3)常温下,向体积为Va mL,pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:_____________;溶液中各离子的浓度按照由大到小排序为_______。
 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=_________(填数字表达式)。
下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是____(填字母)。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V盐酸______V醋酸 ,(填“>”、“<”或“=”下同),反应的最初速率为:υ盐酸_______υ醋酸。
(3)常温下,向体积为Va mL,pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:_____________;溶液中各离子的浓度按照由大到小排序为_______。
(1)(10-5-10-9)mol/L b、c、f (2)< =
(3)Va < Vb c(Na+) = c(CH3COO-) > c(H+) = c(OH-)
(3)Va < Vb c(Na+) = c(CH3COO-) > c(H+) = c(OH-)
(1)在醋酸溶液中其电荷守恒为: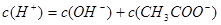 ,由于pH =5即
,由于pH =5即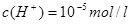 ,所以可得c(CH3COO-)=(10-5-10-9)mol/L;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是:因电离是吸热反应加热电离程度增大;稀释电离程度增大;加入少量0.10 mol·L-1的NaOH溶液能与氢离子反应使醋酸的电离程度增大;
,所以可得c(CH3COO-)=(10-5-10-9)mol/L;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是:因电离是吸热反应加热电离程度增大;稀释电离程度增大;加入少量0.10 mol·L-1的NaOH溶液能与氢离子反应使醋酸的电离程度增大;
(2)等体积且pH均等于3的醋酸和盐酸溶液中,因醋酸是弱酸,所以醋酸的物质的量更大,所以生成氢气的体积:V盐酸小于V醋酸 , 应的最初速率为:υ盐酸=υ醋酸。
(3)若两都等体积反应,则醋酸过量溶液显酸性,而现要使溶液显中性,即Va < Vb;溶液中各离子的浓度按照由大到小排序为c(Na+) = c(CH3COO-) > c(H+) = c(OH-);
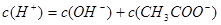 ,由于pH =5即
,由于pH =5即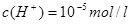 ,所以可得c(CH3COO-)=(10-5-10-9)mol/L;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是:因电离是吸热反应加热电离程度增大;稀释电离程度增大;加入少量0.10 mol·L-1的NaOH溶液能与氢离子反应使醋酸的电离程度增大;
,所以可得c(CH3COO-)=(10-5-10-9)mol/L;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是:因电离是吸热反应加热电离程度增大;稀释电离程度增大;加入少量0.10 mol·L-1的NaOH溶液能与氢离子反应使醋酸的电离程度增大;(2)等体积且pH均等于3的醋酸和盐酸溶液中,因醋酸是弱酸,所以醋酸的物质的量更大,所以生成氢气的体积:V盐酸小于V醋酸 , 应的最初速率为:υ盐酸=υ醋酸。
(3)若两都等体积反应,则醋酸过量溶液显酸性,而现要使溶液显中性,即Va < Vb;溶液中各离子的浓度按照由大到小排序为c(Na+) = c(CH3COO-) > c(H+) = c(OH-);

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
 NH4++NH2—电离平衡关系,两离子的平衡浓度均为1×10-15mol·L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
NH4++NH2—电离平衡关系,两离子的平衡浓度均为1×10-15mol·L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
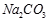 ②
②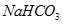 ?③
?③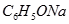 ? ④
? ④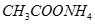 ⑤
⑤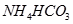 (已知酸性
(已知酸性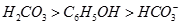 。)
。) CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是( )
CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是( )