题目内容
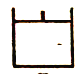
【题目】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是__,C的电子式为__。
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是__。过量的A的水溶液与AlCl3溶液反应离子方程式为__。
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为__mol。
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是__,B与KMnO4溶液反应离子方程式为__。
【答案】第三周期第IA族 ![]() 4NH3+5O2=4NO+6H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 2.4 2SO2+O2
4NH3+5O2=4NO+6H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 2.4 2SO2+O2![]() =2SO3 5SO2+2MnO42-+2H2O=5SO42-+2Mn2++4H+
=2SO3 5SO2+2MnO42-+2H2O=5SO42-+2Mn2++4H+
【解析】
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体,则A为Na,B为Na2O,C为Na2O2,D为NaOH;
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体,则A为NH3,B为NO,C为NO2,D为HNO3;
(3) 若B为能使品红溶液褪色的无色刺激性的气体,B为SO2,C为SO3,D为H2SO4,以此解答。
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体,则A为Na,B为Na2O,C为Na2O2,D为NaOH,A的元素在周期表中的位置是第三周期第IA族,Na2O2的电子式为:![]() ;
;
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体,则A为NH3,B为NO,C为NO2,D为HNO3;
①A→B反应的化学方程式是:4NH3+5O2=4NO+6H2O;过量的NH3的水溶液与AlCl3溶液反应生成氢氧化铝,离子方程式为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+;
②A与C反应生成E和水,E是空气中含量最多的气体N2,化学方程式为:8NH3+6NO2![]() =7N2+12H2O,19.6g N2的物质的量为
=7N2+12H2O,19.6g N2的物质的量为![]() =0.7mol,则消耗NH3的物质的量为0.8mol,NH3中N的化合价从-3价上升到0价转移3个电子,共转移电子的物质的量为0.8mol
=0.7mol,则消耗NH3的物质的量为0.8mol,NH3中N的化合价从-3价上升到0价转移3个电子,共转移电子的物质的量为0.8mol![]() 3=2.4mol;
3=2.4mol;
(3) 若B为能使品红溶液褪色的无色刺激性的气体,B为SO2,C为SO3,D为H2SO4,B→C反应的化学方程式是:2SO2+O2![]() 2SO3;SO2与KMnO4溶液反应生成硫酸,离子方程式为:5SO2+2MnO42-+2H2O=5SO42-+2Mn2++4H+。
2SO3;SO2与KMnO4溶液反应生成硫酸,离子方程式为:5SO2+2MnO42-+2H2O=5SO42-+2Mn2++4H+。

【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1molL﹣1 的 NaOH 溶液中,溶液的 pH=_____。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____, 由水电离出的 c(OH﹣)=_____molL﹣1。
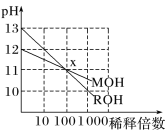
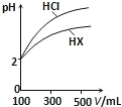
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____(填“强酸”或“弱酸”),理由是_____。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________(填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________倍。