题目内容
下列物质中,属于强电解质的是 (填序号,下同);属于弱电解质的是 ;属于非电解质的是 。
①氨气;②氨水;③盐酸;④醋酸(CH3COOH);⑤硫酸钡;⑥氯化银;⑦氯化钠溶液;⑧二氧化碳;⑨醋酸铵;⑩氢气
⑤⑥⑨ ④ ①⑧
【解析】强、弱电解质的区别在于其溶于水的部分在水溶液中能否完全电离,电解质和非电解质都指的是化合物。氨气(NH3)、二氧化碳(CO2)本身不电离,又是化合物,所以是非电解质;氢气是单质,既不是电解质也不是非电解质;氯化钠溶液、氨水、盐酸都是混合物,既不是电解质也不是非电解质;大多数酸、碱、盐是电解质,所以醋酸(CH3COOH)、硫酸钡、氯化银、醋酸铵都是电解质,其中,硫酸钡(BaSO4)、氯化银(AgCl)由于溶解度小,所以离子浓度小,虽然溶液导电性弱,但溶解的部分完全电离,所以是强电解质;CH3COOH、NH3·H2O在水溶液中只能部分电离,属于弱电解质,但两者反应的产物醋酸铵(CH3COONH4)在水溶液中完全电离,是强电解质。

活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
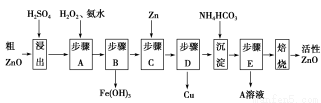
已知:几种离子生成氢氧化物沉淀时的pH如表:
待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是 ,该步骤需控制溶液pH的范围是 。
(2)A溶液中主要含有的溶质是 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为 mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。