题目内容
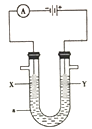
【题目】三氯氧磷(POCl2)是重要的基础化工原料,广泛用于制药、染化。塑胶助剂等行业。某兴趣小组模拟PCl3直接氧化法制备POCl3,实验装置设计如下:

有关物质的部分性质如下表:
熔点/℃ | 沸点/℃ | 其他 | |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
回答下列问题:
(1)装置A中发生反应的化学方程式为___________________________。
(2)B装置的作用除观察O2的流速之外。还有__________________________。
(3)C装置控制反应在60℃~65℃进行,其主要目的是_______________________。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取xg 产品于锥形瓶中,加入足量NaOH 溶液,待完全反应后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000mol/L 的AgNO3容液40.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用cmol/LNH4SCN 溶液滴定过量Ag+至终点,记下所用 体积VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是________________(填标号)。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②Cl元素的质量百分含量为(列出算式)____________________。
③步骤Ⅲ加入硝基苯的目的是_________________,如无此操作,所测Cl元素含量将会____________填“偏大”“ 偏小”或“不变”)。
【答案】 2Na2O2+2H2O=4NaOH+O2↑(或2H2O2![]() 2H2O+O2↑) 平衡气压、干燥O2(或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质) 加快反应速率,同时防止PCl3气化,逸出损失 b
2H2O+O2↑) 平衡气压、干燥O2(或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质) 加快反应速率,同时防止PCl3气化,逸出损失 b ![]() ×100% [或
×100% [或![]() %] 3 防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀,导致多消耗NH4SCN溶液偏小
%] 3 防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀,导致多消耗NH4SCN溶液偏小
【解析】(1)装置A中应该为不加热条件下制备氧气,故可以利用过氧化钠与水反应或双氧水在二氧化锰催化剂下分解生成氧气,发生反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑(或2H2O2![]() 2H2O+O2↑);(2)B装置的作用除观察O2的流速之外。还有平衡气压、干燥O2或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质;(3)根据图表信息可知,PCl3沸点较低,一旦温度过高,PCl3会大量挥发,从而导致产量降低;但是温度过低,反应速率会变慢,因此C装置要控制反应在60℃~65℃进行;(4)①实验中用NH4Fe(SO4)2溶液滴定过量银离子,当银离子反应完全,溶液中存在SCN-,遇铁离子生成红色配合物溶液颜色为红色,所以用NH4Fe(SO4)2做指示剂,答案选b;②根据反应SCN-+Ag+= AgSCN↓可知,硝酸银溶液中剩余硝酸银的量为,根据反应Cl-+Ag+= AgCl↓可知,与氯离子反应的硝酸银的量为0.1000
2H2O+O2↑);(2)B装置的作用除观察O2的流速之外。还有平衡气压、干燥O2或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质;(3)根据图表信息可知,PCl3沸点较低,一旦温度过高,PCl3会大量挥发,从而导致产量降低;但是温度过低,反应速率会变慢,因此C装置要控制反应在60℃~65℃进行;(4)①实验中用NH4Fe(SO4)2溶液滴定过量银离子,当银离子反应完全,溶液中存在SCN-,遇铁离子生成红色配合物溶液颜色为红色,所以用NH4Fe(SO4)2做指示剂,答案选b;②根据反应SCN-+Ag+= AgSCN↓可知,硝酸银溶液中剩余硝酸银的量为,根据反应Cl-+Ag+= AgCl↓可知,与氯离子反应的硝酸银的量为0.1000![]() 40
40![]() 10-3-cV
10-3-cV![]() 10-3=4
10-3=4![]() 10-3-cV
10-3-cV![]() 10-3mol;Cl元素的质量百分含量为
10-3mol;Cl元素的质量百分含量为![]() ×100%或
×100%或![]() %;③步骤Ⅲ加入硝基苯的目的是防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀,导致多消耗NH4SCN;氯化银和AgSCN的Ksp相差不大,在溶液中存在沉淀转化,所以加入有机物覆盖沉淀表面阻断氯化银溶解平衡的转化;若无此操作则第Ⅳ消耗NH4SCN溶液偏高,计算出氯元素含有偏少。
%;③步骤Ⅲ加入硝基苯的目的是防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀,导致多消耗NH4SCN;氯化银和AgSCN的Ksp相差不大,在溶液中存在沉淀转化,所以加入有机物覆盖沉淀表面阻断氯化银溶解平衡的转化;若无此操作则第Ⅳ消耗NH4SCN溶液偏高,计算出氯元素含有偏少。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案