题目内容
4.某元素在自然界中有两种同位素组成,其原子个数比为2.44:1.05,第一种同位素的原子核内有29个质子和34个中子,第2种同位素原子核中的中子数比第一种多2个,该元素平均相对原子质量是( )| A. | 63.00 | B. | 63.60 | C. | 64.00 | D. | 65.00 |
分析 同种元素的质子数相同,先根据质量数=质子数+中子数,然后利用各自的原子个数之比求出平均相对原子质量;
解答 解:第1种同位素的原子核内有29个质子和34个中子,所以它的相对原子质量=29+34=63,第2种同位素原子核中的中子数比第一种多2个,质子数为29,所以它的相对原子质量=29+34+2=65,又因为原子个数比为2.44:1.05,所以该元素的平均原子量=$\frac{63×2.44+65×1.05}{2.44+1.05}$=63.60,故选B.
点评 本题主要考查元素的相对原子质量和核素的相对原子质量之间的关系,难度不大,掌握计算方法即可完成.

练习册系列答案
相关题目
15.如图为铜锌原电池示意图,下列说法中正确的是( )


| A. | 锌片逐渐溶解 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 电解质溶液的pH保持不变 |
12.下列物质属于强电解质的是( )
| A. | NaCl溶液 | B. | BaSO4 | C. | Cu | D. | HClO |
19.下列事实与胶体性质无关的是( )
| A. | 向豆浆中加入盐卤做豆腐 | |
| B. | 钢笔使用不同牌子的墨水堵塞 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一束光亮的通路 | |
| D. | 向石灰水中通入二氧化碳气体产生白色浑浊 |
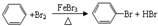 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应.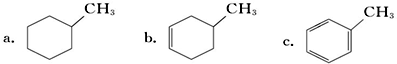
 c.
c.
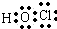 .家用消毒剂与洁厕剂(主要成分是含N的无氧酸)不宜混用,以防产生刺激性的有毒气体,请写出该反应的离子方程式:ClO-+Cl-+2H+═Cl2↑+2H2O
.家用消毒剂与洁厕剂(主要成分是含N的无氧酸)不宜混用,以防产生刺激性的有毒气体,请写出该反应的离子方程式:ClO-+Cl-+2H+═Cl2↑+2H2O .
.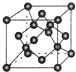 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题: