题目内容
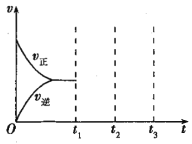
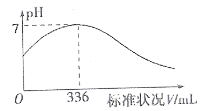
【题目】短周期主族元素X、Y、Z、R的原子序数依次增大,X是宇宙中含量最多的元素,Y原子最外层电子数等于内层电子数的2倍。向100 mL X2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如图。下列说法正确的是( )
A.X2R溶液的浓度为0.03 molL1
B.最简单气态氢化物的稳定性:Y>Z>R
C.X、Y、Z三种元素形成的化合物一定易溶于水
D. RZ2分别通入到X2R、Ba(NO3)2溶液中,均会产生沉淀
【答案】D
【解析】
短周期主族元素X、Y、Z、R的原子序数依次增大,X是宇宙中含量最多的元素,X为H,Y原子最外层电子数等于内层电子数的2倍,Y为C,向100 mL X2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如图,则说明是H2S通入SO2,则Z为O,R为S。
A. 根据2H2S + SO2 = 3S↓+ 2H2O,加入SO2气体体积336mL即0.015mol,溶液pH =7,即消耗H2S物质的量为0.03mol,因此X2R溶液的浓度为![]() ,故A错误。
,故A错误。
B. 非金属性越强,最简单气态氢化物的稳定性越强,即稳定性H2O>CH4,故B错误;
C. H、C、O三种元素形成的化合物,如果属于酯等,则不溶于水,故C错误;
D. SO2通入到H2S有黄色沉淀生成,SO2通入到Ba(NO3)2溶液中生成硫酸钡沉淀,故D正确。
答案为D。

【题目】草酸钴用途广泛,可用于指示剂和催化剂的制备。用含钴废料(主要成分为![]() ,还含有一定量的
,还含有一定量的![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等)制备草酸钴晶体
等)制备草酸钴晶体![]() 的工业流程如下图所示。请回答下列问题:
的工业流程如下图所示。请回答下列问题:
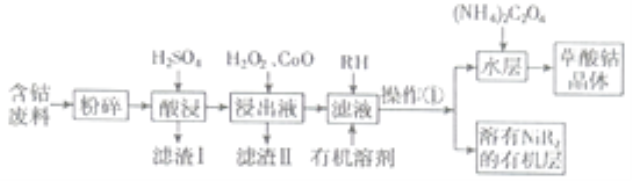
已知:①草酸钴晶体难溶于水
②![]() 为有机物(难电离)
为有机物(难电离)
③相关金属离子![]() 形成氢氧化物沉淀的
形成氢氧化物沉淀的![]() 范围如下:
范围如下:
金属离子 |
|
|
|
|
开始沉淀的 | 7.5 | 2.7 | 3.4 | 6.9 |
沉淀完全的 | 9.0 | 3.7 | 4.7 | 8.9 |
(1)滤渣Ⅰ的成分_______。
(2)![]() 是一种绿色氧化剂,写出加入
是一种绿色氧化剂,写出加入![]() 后溶液中发生的主要反应的离子方程式______。
后溶液中发生的主要反应的离子方程式______。
(3)加入氧化钴调节浸出液的![]() 的范围是______。
的范围是______。
(4)加入有机溶剂的目的是______。
(5)若仅从沉淀转化角度考虑,能否利用反应![]() 将
将![]() 转化为
转化为![]() ____(填“能”或“不能”),说明理由:______。(已知
____(填“能”或“不能”),说明理由:______。(已知![]() ,
,![]() )
)
(6)为测定制得的草酸钴晶体样品的纯度,现称取样品![]() ,先用适当试剂将其转化,稀释后得到纯净的草酸铵溶液
,先用适当试剂将其转化,稀释后得到纯净的草酸铵溶液![]() 。移取
。移取![]() 该溶液加入过量的稀硫酸酸化,用
该溶液加入过量的稀硫酸酸化,用![]() 高锰酸钾溶液滴定,当溶液由__________(填颜色变化),消耗高锰酸钾溶液
高锰酸钾溶液滴定,当溶液由__________(填颜色变化),消耗高锰酸钾溶液![]() ,计算草酸钴晶体样品的纯度为__________
,计算草酸钴晶体样品的纯度为__________![]() 。(用含
。(用含![]() 、
、![]() 、
、![]() 的代数式表示)(已知
的代数式表示)(已知![]() 的摩尔质量为
的摩尔质量为![]() )
)
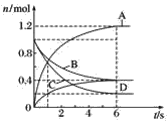
【题目】以NaClO为有效成分的“84”消毒液在抗击新冠疫情的消杀工作中起到了重要作用。某研究小组设计下列实验探究NaClO的性质。
(已知:电离常数:![]() :
:![]() ,
,![]() ;
;![]() )
)
实验 | 装置 | 试剂(少量) | 预测可能的现象 |
① |
| 酚酞 | 无色溶液最终呈红色 |
② |
| 无明显现象 | |
③ | 淀粉 | 无色溶液立即变蓝 | |
④ |
| 溶液略呈浅绿色 |
结合上述实验探究,预测的现象以及解释均正确的是( )
A.实验①:NaClO溶液呈碱性:![]()
B.实验②:NaClO可用于制得![]()
C.实验③:NaClO具有氧化性:![]()
D.实验④:NaClO具有还原性:![]()
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为_____。
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为_____。
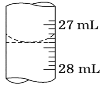
乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(4)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______(保留四位有效数字)。
(5)下列哪些操作会使测定结果偏高_____ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是________。
【题目】一种从含Br-废水中提取Br2的过程,包括过滤、氧化、正十二烷萃取及蒸馏等步骤。已知:
Br2 | CCl4 | 正十二烷 | |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
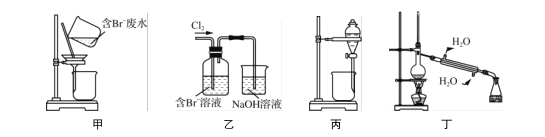
下列说法正确的是( )
A. 用甲装置过滤时,需不断搅拌
B. 用乙装置将Br-氧化为Br2
C. 丙装置中用正十二烷而不用CCl4,是因为其密度小
D. 可用装置丁进行蒸馏,先收集正十二烷再收集Br2