��Ŀ����
����Ŀ��ijͬѧ�������������طֽ���O2�ⶨ��״��������Ħ�������̽��ʵ�顣
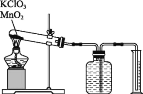
ʵ�鲽������:�����Ӻ�ʵ��װ��,���װ�õ������ԡ���������������ط�ĩ�������������̷�ĩ��Ͼ���,���������Թ���,ȷ�����Թܺ�ҩƷ��������Ϊ15.95g��������,��ʼ��Ӧ,ֱ���������������Ϊֹ��������������Ͳ��ˮ�����Ϊ285.0mL,����ɱ�״�������������Ϊ279.7mL����ȷ�����ԹܺͲ����������Ϊ15.55g����������ʵ�����,�ش��������⡣
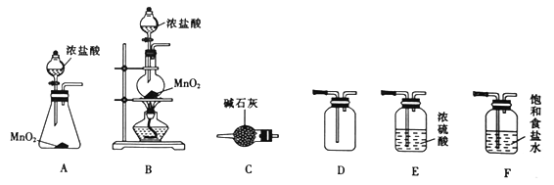
��1����μ��װ�õ�������?________��
��2�������Dz����ռ��������������������ļ�������:��ʹ�Թܺ��ƿ�����嶼��ȴ������;��_____;����ȡ��Ͳ��Һ����������������ʵ�����ʱ,�����Ӷ���,���ȡ���������__ (����ƫ������ƫС��������Ӱ����)��
��3��ʵ������в������������ʵ�����______mol��ʵ���ñ�״����������Ħ�������__ (����С�������λ)��
���𰸡������ƿ��ע��ˮ,��������,��װ��ͼ���Ӻ�װ��,���ֽ��Թܵײ�����,���۲쵽���ƿ�г���������Һ������,�ɿ��ֺ�,��һ������������ڵ�Һ���½�,��֤����װ�ò�©�� ������Ͳ�ĸ߶�ʹ���ƿ����Ͳ�ڵ�Һ��߶���ͬ ƫС 0.0125 22.38 L��mol-1
��������
(1)װ�������Լ����ԭ����:ͨ�����巢�����븽���Һ�幹�ɷ����ϵ�����ݸı���ϵ��ѹǿʱ����������(�����ݵ����ɡ�ˮ�����γɡ�Һ���������)���ж�װ�������ԣ�
(2)Ҫȷ��������������뱣����Ͳ����������¶Ⱥ�ѹǿ��ȣ�����ڶ�ȡ��Ͳ����������֮ǰ��Ӧʹ�Թܺ���Ͳ�ڵ����嶼��ȴ�����£��ٵ�����Ͳ����Һ��߶�ʹ֮��ͬ�����Ӷ���ƫС��
(3)�Թܺ�ҩƷ��ʵ��ǰ��������Ϊ���ɵ���������������������Ħ����n=V/Vm���㡣
(1)װ�������Լ����ԭ����:ͨ�����巢�����븽���Һ�幹�ɷ����ϵ�����ݸı���ϵ��ѹǿʱ����������(�����ݵ����ɡ�ˮ�����γɡ�Һ���������)���ж�װ�������ԣ����ȸ��������ȡ����ʱ�ļ���װ�������Եķ���Ϊ�������ƿ��ע��ˮ��������Ƥ������װ��ͼ���Ӻ�װ�ã����ֽ��Թܵײ����ȣ����۲쵽���ƿ�г���������Һ���������ɿ��ֺ�,��һ�᳤�������ڵ�Һ���½�����֤����װ�ò�©����
�ʴ��ǣ������ƿ��ע��ˮ��������������װ��ͼ���Ӻ�װ�ã����ֽ��Թܵײ����ȣ����۲쵽���ƿ�г���������Һ���������ɿ��ֺ�,��һ������������ڵ�Һ���½�����֤����װ�ò�©����
(2)��Ϊ�ų�����������Ҫ���ų���ˮ����������ģ�����Ӧǰ�����Ͳ�¶��Dz�ͬ�ģ���˷�Ӧ��ֹӦ����ֹͣ���ȣ�����ϵ�ָ�������ʱ����ȡ�����ܣ���һ��������ͨ����ʵ�鲻ͬ������ֹͣ����ʱ���ܵij���Ҫ������Ͳ�ڵ�Һ�棬��ʱ��ʹ��ȡ�����ܶ�ֹͣ���ȣ�Ҳ�������ˮ�ĵ�����ֹͣ���ȡ��ص����º���Ͳ�����Ե�����Ͳ�ڵ�Һ����ˮ��һ�£���ʱ��Ͳ������ѹǿҲΪ����ѹ������������ȷ�ģ����Բ���˳��Ϊ:��ʹ���嶼��ȴ�����£��ڵ�����Ͳ����Һ��߶�ʹ֮��ͬ���۶�ȡ��Ͳ������������������Ͳ�Ľṹ��֪�����Ӷ���ʹ�ö���ƫС��
�ʴ���: ������Ͳ�ĸ߶�ʹ���ƿ����Ͳ�ڵ�Һ��߶���ͬ��ƫС��
(3)���ɵ�����������m=15.95-15.55=0.4g���������ʵ���n=m/M=0.4/32=0.0125mol�����������V=279.7mL=0.2797L��������Ħ�����Vm=V/n=0.2797L/0.0125mol=22.38 L��mol-1��
�ʴ���: 0.0125�� 22.38L��mol-1��

����Ŀ��Ϊ�˲ⶨʵ���ҳ��ڴ�ŵ�Na2SO3����Ĵ��ȣ�ȷ��ȡw g������Ʒ�����250 mL��Һ���������������ʵ�鷽����
����I��ȡ25.00 mL������Һ�����������������ữ��BaCl2��Һ������I��ϴ������������������õ�����������Ϊm1 g
��������ȡ25.00 mL������Һ����a mol/L ������KMnO4��Һ���еζ���(5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O)
�ζ�����ʵ������ | 1 | 2 | 3 | 4 |
������Һ���/mL | 25.00 | 25.00 | 25.00 | 25.00 |
�ζ��ܳ�����/mL | 0.00 | 0.20 | 0.10 | 0.15 |
�ζ���ĩ����/mL | 19.95 | 20.20 | 19.15 | 20.20 |
ʵ��������¼���������±���
��1������250 mL Na2SO3��Һʱ�������õ���ʵ�������У��ձ�������������ͷ�ιܡ���Ͳ��ҩ��_________��____________��
��2������IΪ________������Ϊ____________
��3������I������жϼ�����Ȼ����Ѿ�����_____________���ڷ������еζ��յ���жϷ�����________________��
��4�����ݷ��������ṩ�����ݣ�����Na2SO3�Ĵ���Ϊ_________��
��5������ʵ���У����ڲ����������������������ȷ����_________
A.����I����û��ϴ�Ӳ�����ʵ������ƫС
B.����I����û�в�������ʵ������ƫ��
C.�������У��ζ����ڵζ�ǰ�����ݣ��ζ���������ݣ�ʵ����ƫС
D.�������У��ζ��յ�ʱ���Ӷ�����ʵ����ƫ��