��Ŀ����
����Ŀ���Ը��������Ҫ�ɷ�ΪFe(CrO2)2������Al2O3��Fe2O3��SiO2�����ʣ�Ϊ��Ҫԭ�������ظ����ƾ��壨Na2Cr2O7��2H2O������Ҫ����������ͼ��
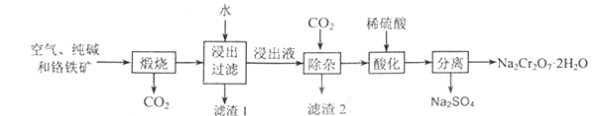
��1�����չ����У��������е�Al2O3�봿�Ӧ�Ļ�ѧ����ʽΪ��____��
��2������1�ijɷ�Ϊ_____������2�ijɷ�Ϊ_____��
��3���ù�����ij�ֲ�����������ã������ʵĻ�ѧʽΪ��_____��
��4���ữʱ�����ķ�ӦΪ��2CrO42-+2H+![]() Cr2O72-+H2O����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��CrO42-��
Cr2O72-+H2O����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��CrO42-��![]() ת��ΪCr2O72-��
ת��ΪCr2O72-��
���ữʱ������Ӧ��ƽ�ⳣ���ı���ʽΪK=_____��
���ữ��������Һ��c(Cr2O72-)=____��
��3�������йع��ұ�����CrO42-�ķ�ˮҪ����ѧ������ʹ��Ũ�Ƚ���5.0��10-7mol��L-1���²����ŷš���CrO42-�ķ�ˮ����ͨ�����������ַ�����
�ٳ���������������Ա�������BaCrO4������Ksp(BaCrO4)=1.2��10-10�ݣ��ټ�������������δ��������Ba2+����������Ա��κ�ķ�ˮ��Ba2+��Ũ��Ӧ��С��____mol��L-1��������ˮ�������ܴﵽ�����ŷű���
�ڻ�ԭ����CrO42-![]() Cr3+
Cr3+![]() Cr(OH)3��д������������CrO42-���̷���Ӧ�����ӷ���ʽ____��
Cr(OH)3��д������������CrO42-���̷���Ӧ�����ӷ���ʽ____��
���𰸡�Al2O3+Na2CO3![]() 2NaAlO2+CO2�� Fe2O3 H2SiO3��Al(OH)3 CO2
2NaAlO2+CO2�� Fe2O3 H2SiO3��Al(OH)3 CO2 ![]() 0.25mol��L-1 2.4��10-4
0.25mol��L-1 2.4��10-4 ![]()
��������
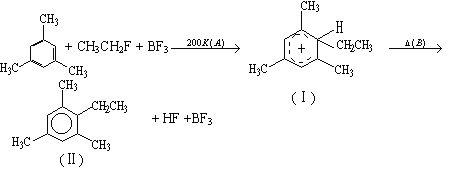
������[��Ҫ�ɷ�ΪFe(CrO2)2������Al2O3��Fe2O3��SiO2������]���������������ڸ�����������������Fe2O3��Na2CrO4��NaAlO2��Na2SiO3��CO2������ˮ��������ʱ��Fe2O3������ˮ������������Һ��ͨ��CO2�����ɲ�����ˮ��H2SiO3��Al(OH)3����Һ����Ҫ�ɷ�ΪNa2CrO4��̼������(��̼����)������ϡ�����Na2CrO4ת��ΪNa2Cr2O7��̼������(��̼����)ת��Ϊ�����ƣ�Ȼ������õ�Na2Cr2O7��2H2O���Դ˽���⡣
��1����������ͼ��֪�����չ����У��������е�Al2O3�봿�Ӧ������CO2��Ȼ������Ԫ���غ���ƽ���û�ѧ����ʽΪ��Al2O3+Na2CO3![]() 2NaAlO2+CO2����
2NaAlO2+CO2����
��2��������������֪������1ΪFe2O3������2ΪH2SiO3��Al(OH)3��
��3��������ͼ��֪����ѭ�����õ�����ΪCO2��
��4���ٸ���ƽ�ⳣ�����壺���滯ѧ��Ӧ�ﵽƽ��״̬ʱ�������뷴Ӧ���Ũ�ȣ�����ʽϵ���ݴη����˻��Ȼ�Ӧ�����뷴Ӧ�����Ũ�ȣ�����ʽϵ���ݴη����˻��ȿ�֪���÷�Ӧƽ�ⳣ��Ϊ��![]() ��
��
����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��![]() ��
��![]() ת��Ϊ
ת��Ϊ![]() ��˵����Ԫ����
��˵����Ԫ����![]() ת��Ϊ
ת��Ϊ![]() �������غ��й�ϵʽ��
�������غ��й�ϵʽ��
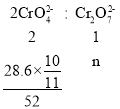
��n=0.25mol��n(![]() )ʣ��=0.05mol������ữ��������Һ��c(
)ʣ��=0.05mol������ữ��������Һ��c(![]() )=
)=![]() =0.25molL-1��
=0.25molL-1��
��3����![]() =5��10-7��c(Ba2+)=1.2��10-10�����c(Ba2+)=2.4��10-4mol/L��
=5��10-7��c(Ba2+)=1.2��10-10�����c(Ba2+)=2.4��10-4mol/L��
������������![]() ���������ӷ�Ӧ����Cr3+��Fe3+��ˮ������������ԭ��Ӧ��ʧ�����غ㡢����غ��Լ�ԭ���غ��֪�䷴Ӧ�����ӷ���ʽΪ��
���������ӷ�Ӧ����Cr3+��Fe3+��ˮ������������ԭ��Ӧ��ʧ�����غ㡢����غ��Լ�ԭ���غ��֪�䷴Ӧ�����ӷ���ʽΪ��![]() ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij�Ͼ���ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ���������ͼ��
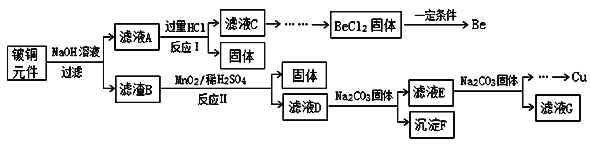
��֪��I���롢��Ԫ�ػ�ѧ�������ƣ�
�����²�����������ܶȻ����������
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�����(Ksp) | 2.2��10��20 | 4.0��10��38 | 2.1��10��13 |
(1)��ҺA����Ҫ�ɷֳ�NaOH��Na2BeO2�⣬����___________(�ѧʽ)��д����ӦI��Na2BeO2��������ᷴӦ�����ӷ���ʽ��________��
(2)��ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ_______(����ĸ)
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH d.����������HCl e.ϴ�� f.����
(3)MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��___________������ŨHNO3�ܽ�������ȱ����_______(��дһ��)��
(4)��ҺD��c(Cu2+)��2.2mol��L��1��c(Fe3+)��8.0��10��3mol��L��1��c(Mn2+)��0.01mol��L��1����μ���Na2CO3��Һ����pH�ɽ���ת��������������η��룬���ȳ�������_______(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����______��